
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3.2g | B.4.8g | C.6.4g | D.10.8g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
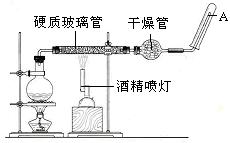
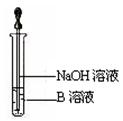
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该晶体中一定含有SCN— | B.氧化性:Fe3+> Cl2 |
| C.Fe2+与SCN—不能形成红色物质 | D.Fe2+被氯水氧化成Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 与用不含O2的蒸馏水配制的NaOH溶液反应制备。
与用不含O2的蒸馏水配制的NaOH溶液反应制备。 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若n=5.1,则m的值可能为9.8 |
| B.若n=5.1,则参加反应的硝酸的物质的量为0.4 mol |
| C.若n=5.1,则加入的NaOH溶液的体积为150 mL |
D.若n =5.1,则被还原的硝酸的物质的量为0.1 mol =5.1,则被还原的硝酸的物质的量为0.1 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在FeSO4中滴入KSCN溶液,溶液显红色 |
| B.铁位于元素周期表中第4周期Ⅷ族 |
| C.在化合物中,铁元素常呈现为+2、+3价 |
| D.通常情况下,铁丝在氯气里燃烧时生成FeCl3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.无法计算原混合物的质量a |
| B.原混合物中n(Fe)∶n(Fe2O3)=2∶1 |
| C.向溶液中滴入KSCN溶液,显红色 |
| D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com