
已知HClO是比H2CO3还弱的酸,氯水中存在下列平衡:Cl2+H2O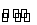 HCl
HCl
+HClO;HClO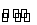 H++ClO-,达平衡后:
H++ClO-,达平衡后:
(1)要使HClO的浓度增加,可加入下列物质(填代号)________。
A.SO2 B.CaCO3 C.HCl D.NaOH
(2)由此说明在实验室里可用排饱和食盐水收集Cl2的理由是_______________。
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.NaCl溶液在电流的作用下电离成Na+和Cl-
B.溶于水后能电离出氢离子的化合物都是酸
C.二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质
D.硫酸钡难溶于水,但硫酸钡属于强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关能源利用的措施或叙述错误的是( )
A.光催化还原水制氢比电解水制氢更节能环保、更经济
(2014·浙江理综,7A)
B.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
(2014·天津理综,3C)
C.大量燃烧化石燃料是造成雾霾天气的一种重要因素
(2014·天津理综,1C)
D.向汽油中添加甲醇后,该混合燃料的热值不变
(2014·浙江理综,7D)
查看答案和解析>>
科目:高中化学 来源: 题型:
在微生物作用的条件下,NH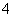 经过两步反应被氧化成NO
经过两步反应被氧化成NO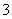 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
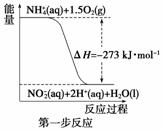
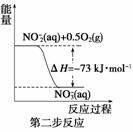
①第一步反应是________反应(选填“放热”或“吸热”),判断依据是________________________________________________________________________。
②1 mol NH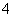 (aq)全部氧化成NO
(aq)全部氧化成NO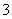 (aq)的热化学方程式是________________________________________________________________________。
(aq)的热化学方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(1)胆矾失水的热化学方程式为CuSO4·5H2O(s)===CuSO4(s)+5H2O(l)
ΔH=+Q1 kJ·mol-1
(2)室温下,无水硫酸铜溶于水的热化学方程式为
CuSO4(s)===Cu2+(aq)+SO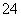 (aq)
(aq)
ΔH=-Q2 kJ·mol-1
(3)胆矾(CuSO4·5H2O)溶于水时溶液温度降低。
则Q1与Q2的关系是(Q1、Q2为正数)( )
A.Q1>Q2 B.Q1=Q2
C.Q1<Q2 D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com