
【题目】某溶液中有较大量的Cl-、CO32-、OH-等三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液
A.①②④②③B.④②①②③C.①②③②④D.④②③②①
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有机合成中的一种重要还原剂—铝氢化钠(NaAlH4),其合成线路如图所示:

(1)已知:AlCl3的熔点为190℃,沸点为178℃,在潮湿空气中会水解。某实验小组利用图所示装置制取无水AlCl3。

①A中所盛装的固体试剂的化学式为________________________。
②装置F的作用是_________________________________________________。
(2)若改变A、B、D 中的试剂就可以用该装置制取NaH,如制取中操作不当,制得的NaH中可能含有的主要杂质为__________(填序号)。
a.Na b.NaOH c.Na2O2 d.Na2CO3
(3)AlCl3与NaH 反应时,需将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末上,此反应中NaH的转化率较低的原因是____________________________________。
(4)铝氢化钠遇水发生剧烈反应,甚至爆炸,其反应的化学方程式为__________________________。
(5)现设计如图所示四种装置,测定铝氢化钠粗产品的纯度(只含NaH杂质)。

从简约性、安全性和准确性考虑,最适宜的装置是_________(填编号)。铝氢化钠与水完全反应,读气体体积时需冷却至室温,则冷却至室温的标志是__________________________________。
若称取24.0g样品与水完全反应后,测得生成气体在标准状况下的体积为38.08L,则样品中铝氢化钠的质量分数为_______________。(结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞分子的叙述,正确的是( )
A. 携带遗传信息是核酸的唯一功能
B. 叶肉细胞中缺乏 Mg 元素,则影响叶绿素合成
C. 氨基酸的空间结构是蛋白质多样性的原因
D. 等质量脂肪氧化分解比糖释放能量多是因为脂肪分子中氧含量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列各组微粒或物质:
A、O2和O3
B、 ![]() 和
和 ![]()
C、CH3CH2CH2CH3和 ![]()
D、 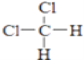 和
和 
E、CH3CH2CH2CH3和 ![]()
(1)________组两种微粒互为同位素;
(2)________组两种物质互为同素异形体;
(3)________组两种物质属于烃;
(4)________组两物质互为同分异构体;
(5)________组两物质是同一物质.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铝片与1molL-1稀盐酸反应制取氢气时,下列措施不能使氢气生成速率增大的是
A.对该反应体系加热B.用浓硫酸代替稀盐酸
C.加入少量硫酸铜溶液D.加入少量1molL-1硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 是短周期中原子序数依次增大的四种元素。X可以分别与Y、Z、W 结合生成甲、乙、丙三种相同质子数的分子;相关物质之间的转化关系如图所示,已知丁是无色气体,遇空气显红棕色。下列说法正确的是
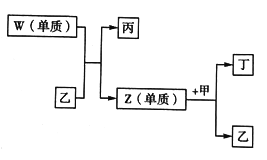
A. 原子半径的大小:W>X>Y>Z B. 单质的稳定性:X>Y>Z>W
C. 简单氢化物的沸点:Y>Z>W D. X 与Y、Z 均可形成原子个数比为2: 1的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下图所示化合物的说法不正确的是 ( ) 
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1mol该化合物最多可以与3molNaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列几个实验,可快速制取实验室所需的少量气体,并进行相关性质实验。(实验装置如图所示)

(1)若B中是生石灰,C中盛有AlCl3溶液,将A中液体逐滴加入B内,实验中观察到C溶液中出现白色沉淀。则A中液体的是_______(填名称),C中发生反应的离子方程式为_________________________。
(2)若要制O2,B为黑色固体,A中的试剂是_________(填化学式),C中盛有FeCl2和KSCN的混合液,旋开分液漏斗的开关后,发现C中溶液变为血红色,同时生成红褐色沉淀。写出C中发生氧化还原反应的离子方程式_______。
(3)已知氧化性强弱:KMnO4>Cl2>KIO3>I2。若A中装有浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,C中的现象是_____________,继续反应一段时间后,发现C中溶液的颜色褪去,这是因为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学分析法测得某有机物的化学成分及含量如下表所示,则该物质最可能是()
元素 | C | O | N | H | S | Fe |
含量(%) | 92.393 | 3.518 | 2.754 | 1.214 | 0.006 | 0.006 |
A. 核酸 B. 脂肪 C. 蛋白质 D. 糖类
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com