
| A. | 明矾、氯化铁晶体可用于净水 | |
| B. | 实验室通常可使用热的纯碱溶液去除油污 | |
| C. | 实验室配制FeCl3溶液时可加入少量盐酸 | |
| D. | 直接加热CuCl2溶液能得到CuCl2固体 |
分析 A、明矾、氯化铁晶体常用于净水是利用铝离子、铁离子水解生成氢氧化铝、氢氧化铁胶体具有吸附作用,可以净水;
B、纯碱溶液中碳酸根离子水解显碱性,加热促进水解,油脂在碱性溶液中水解形成溶于水的物质;
C、氯化铁溶液中铁离子水解显酸性分析;
D、直接加热CuCl2溶液,促进氯化铜的水解,而加热过程中氯化氢气体的挥发,水解平衡正向移动.
解答 解:A、明矾、氯化铁晶体常用于净水是利用铝离子、铁离子水解生成氢氧化铝、氢氧化铁胶体具有吸附作用,可以净水,和盐类水解有关,故A正确;
B、纯碱溶液中碳酸根离子水解显碱性,加热促进水解,油脂在碱性溶液中水解形成溶于水的物质,易于除去,故B正确;
C、氯化铁溶液中铁离子水解显酸性,加入少量盐酸抑制铁离子水解,故C正确;
D、直接加热CuCl2溶液,促进氯化铜的水解,而加热过程中氯化氢气体的挥发,水解平衡正向移动,最后生成氢氧化铜,而不是氯化铜,故D错误;
故选D.
点评 本题考查了盐类水解的分析应用,注意水解过程分析和影响因素的理解,掌握基础是关键,题目较简单.


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:解答题
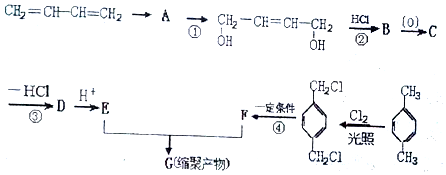
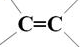 、-COOH.
、-COOH. .
.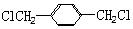 的同分异构体中含有苯环,且苯环上有三个取代基的同分异构体有16种.
的同分异构体中含有苯环,且苯环上有三个取代基的同分异构体有16种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知298K时氢氰酸(HCN)的Ka=4.9×10-10,碳酸的Ka1=4.4×10-7,Ka2=4.7×10-11,据此可推测将氢氰酸加入到碳酸钠溶液中不可能观察到有气泡产生 | |
| B. | 25℃时,将amol•L氨水与0.01mol•L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(CI-),用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
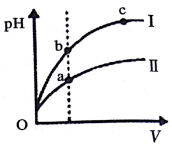
| C. | 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的曲线如图所示.II为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b | |
| D. | 向0.10mol•L-1NaHSO4溶液中通入NH3至溶液pH=7(通入气体对溶液体积的影响可忽略):c(Na+)>c(SO42-)>c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向FeCl3溶液中加入过量铁粉:Fe3++Fe═2Fe2+ | |
| B. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 向稀硫酸中加入 Ba(OH)2 溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
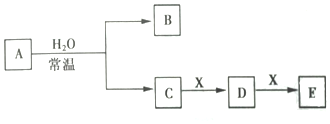
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2O | |
| B. | 铁与稀盐酸混合:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 铜片插入硝酸银溶液中:Cu+2Ag+═Cu2++2Ag | |
| D. | 稀硝酸滴在石灰石上:CaCO3+2H+═Ca2++H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| B. | 目前我国流通的硬币是由合金材料制造的 | |
| C. | 玻璃、水泥、陶瓷都为硅酸盐产品 | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 温度计的水银球应插入到液面以下 | |
| B. | 蒸馏过程中,加入沸石(或碎瓷片)的目的是防止暴沸 | |
| C. | 冷凝管进出水的方向是:上进下出 | |
| D. | 用烧杯接收蒸馏出来的液体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com