
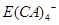 的形式存在,写出E溶于Z溶液的离子方程式:_________________________________________.
的形式存在,写出E溶于Z溶液的离子方程式:_________________________________________.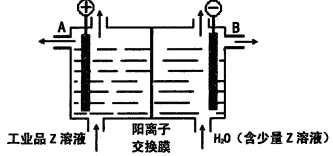
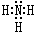 (1分)
(1分)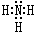 ,Na与液氨反应的方程式为:2Na+2NH3=2NaNH2+H2↑ ,答案:
,Na与液氨反应的方程式为:2Na+2NH3=2NaNH2+H2↑ ,答案: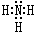 ,2Na+2NH3=2NaNH2+H2↑ ;
,2Na+2NH3=2NaNH2+H2↑ ;

科目:高中化学 来源:不详 题型:单选题
| A.元素W的氢化物的热稳定性比X弱,因为X的氢化物分子间存在氢键 |
| B.四种元素形成的最高价氧化物对应水化物的酸性最强的是W |
| C.他合物YX、ZX2、WX3中化学键类型相同 |
| D.原子半径的大小顺序:r(Y)>r(Z)>r(X)>r(W) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:丙<丁<乙 | B.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
| C.甲、乙、丙的氧化物均为共价化合物 | D.单质的还原性:丁>丙>甲 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素编号 | T | X | Y | Z | W |
| 元素的性质或原子结构情况 | 短周期主族元素中原子半径最大 | 最外层上的电子数比次外层少1个且单质是气体 | 核外共有13种运动状态不同的电子 | 若低温蒸发液态空气,因其沸点较低可先获得它的单质 | 核外有5种不同能量的电子且其中有两个未成对的电子 |
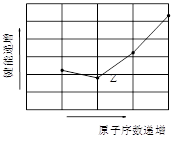
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
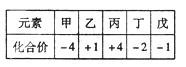
| A.乙的单质中能与水剧烈反应 |
| B.气态氢化物的稳定性:丙>甲 |
| C.丙的氧化物能与戊的氢化物水溶液反应 |
| D.其最高价氧化物对应的水化物的酸性:丁>戊 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关结构和性质 |
| A | A为非金属元素,其一种单质是电的良导体,难熔、质软并有润滑性,可用作电极材料 |
| B | 是蛋白质的组成元素之一,原子核外有三种不同能量的电子,且未成对电子数最多 |
| C | 其单质既能与强酸溶液应又能与强碱溶液反应,其简单离子在第三周期单核离子中半径最小 |
| D | D的高价氯化物的盐溶液常用于印刷电路极电路的“刻蚀” |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCl、HBr、HI的热稳定性依次增强 |
| B.若M+和R2-的核外电子层结构相同,则原子序数:R>M |
| C.同主族元素从上到下,单质的熔点逐渐降低 |
| D.同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 I研究G蛋白偶联受体,下列说法正确的是
I研究G蛋白偶联受体,下列说法正确的是| A.I元素的质量数是131 | B.I元素的中子数是78 |
| C.I原子5p亚层有一个未成对电子 | D.I原子有53个能量不同的电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com