
【题目】下列说法不正确的是( )
A.己烷有4种同分异构体,它们的熔点、沸点各不相同
B.在一定条件下,乙酸乙酯水解、苯与硝酸作用生成硝基苯的反应都属于取代反应
C.油脂皂化反应得到高级脂肪酸盐与甘油
D.聚合物( ![]() )可由单体CH3CH=CH2和CH2=CH2加聚制得
)可由单体CH3CH=CH2和CH2=CH2加聚制得
【答案】A
【解析】解:A.己烷有五种同分异构体,其碳链结构分别为 ![]() 、
、 ![]() 、
、 ![]() 、
、 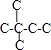 、
、 ![]() ,己烷的同分异构体为不同物质,所以其熔沸点不同,且含有支链越多其熔沸点越低,故A错误; B.乙酸与乙醇发生酯化反应生成乙酸乙酯和水,属于取代反应;在一定条件下,苯与硝酸作用生成硝基苯,是苯中的氢原子被硝基取代,所以都属于取代反应,故B正确;
,己烷的同分异构体为不同物质,所以其熔沸点不同,且含有支链越多其熔沸点越低,故A错误; B.乙酸与乙醇发生酯化反应生成乙酸乙酯和水,属于取代反应;在一定条件下,苯与硝酸作用生成硝基苯,是苯中的氢原子被硝基取代,所以都属于取代反应,故B正确;
C.油脂水解生成高级脂肪酸和甘油,碱性条件下,高级脂肪酸和碱反应生成高级脂肪酸盐和水,所以实际上是油脂在碱性条件下水解生成甘油和高级脂肪酸盐,该反应为皂化反应,故C正确;
D.凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可,所以聚合物( ![]() )的单体是CH3CH=CH2和CH2=CH2 , 故D正确;
)的单体是CH3CH=CH2和CH2=CH2 , 故D正确;
故选A.


科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.电负性的大小顺序为Cl>S>P
B.由于NO3﹣和SO3互为等电子体,所以可以推断NO3﹣的空间构型为平面三角形
C.根据晶格能的大小可以判断MgCl2的熔点比CaCl2高
D.液态HF的沸点比液态HCl的沸点高是因为氢氟键的键能比氢氯键的键能大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在.它的单质和化合物在工农业生产中有着重要的应用.Ⅰ.白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中高温(约1550℃)下通过下面两个反应共熔得到.
①2Ca3(PO4)2(s)+5C(s)=6CaO(s)+P4(s)+5CO2(g)△H1=+Ql kJmol﹣1
②CaO(s)+SiO2(s)=CaSiO3(s)△H2=﹣Q2 kJmol﹣1
(1)写出电炉中发生总反应的热化学方程式Ⅱ.三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料.氯化水解法生产三氯氧磷的流程如图甲: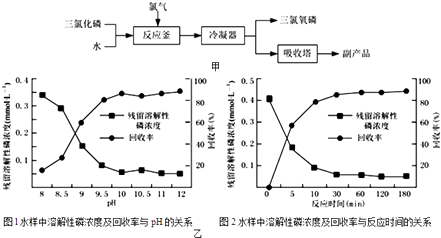
(2)写出氯化水解法生产三氯氧磷的化学方程式为 . 氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水.在废水中先加入适量漂1白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收.
(3)POCl3、H3PO4、H3PO3中磷元素的化合价分别为、、 .
(4)在沉淀前先加入适量漂白粉的作用是 .
(5)Ⅲ.如图乙是不同条件对磷的沉淀回收率的影响图象.处理该厂废水最合适的工艺条件为(选填字母).a.调节pH=9 b.调节pH=10 c.反应时间30min d.反应时间120min
(6)己知磷酸是三元酸,其各级电离常数如下:K1=7.1×10﹣3 K2=6.3×l0﹣8K3=4.2×10﹣13 , 则0.1mol/L的NaH2PO4溶液的pH7(填>,=,<).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中a、b、c表示相应仪器中加人的试剂,可用如图装置制取、净化、收集的气体是( )
编号 | 气体 | a | b | c |
|
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
C | NO | 稀硝酸 | 铜屑 | H2O | |
D | Cl2 | 浓盐酸 | 二氧化锰 | 饱和NaCl溶液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.活化分子碰撞即发生化学反应
B.升高温度会加快反应速率,其主要原因是增加了活化分子碰撞的次数
C.有气体参加的化学反应,若增大压强,可增大活化分子百分数,从而使反应速率增大
D.活化分子间的碰撞不一定是有效碰撞
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况通常是指
A.温度为0℃,压强为101kPaB.温度为20℃,压强为10kPa
C.温度为0℃,压强为202kPaD.温度为20℃,压强为202kPa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:
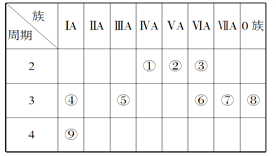
(1)在这些元素中,化学性质最不活泼的是________(填元素符号),②位于元素周期表的第____纵行。
(2)在最高价氧化物的水化物中,碱性最强的化合物的电子式是___________。
(3)④的单质比⑨的单质熔点_______(填“高”或“低”),④⑤⑥⑦的简单离子半径由小到大为___________________。(用序号表示)
(4)①与⑦形成的某种化合物经常用作萃取剂,其结构式为__________,该化合物属于________(填“共价”或“离子”)化合物。④与③形成的淡黄色的固体的阴、阳离子的个数比为_______。
(5)元素③与元素⑥相比,能证明这两种元素非金属性强弱的事实是_______(填选项序号)。
A.常温下③的单质和⑥的单质状态不同
B.③的简单氢化物比⑥的简单氢化物稳定
C.③的简单氢化物的沸点比⑥的简单氢化物的沸点高
D.③的单质能与⑥的简单氢化物反应生成⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将32g铜与100mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2的混合气体标准状况下的体积为11.2L,气体全部逸出后,向溶液中加入VmL n mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的物质的量浓度为 mol/L.(结果须化简)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com