
【题目】(1)在标准状况下,某烃分子的相对分子量为28,一定体积的该烃完全燃烧生成4.48LCO2和3.6g水,该烃的分子式_________________。
(2)顺-1,2-二溴乙烯结构式_________________。
(3)2-丁烯与HCl的加成方程式_______________________________________。
(4)![]() 的系统命名为________________。
的系统命名为________________。
(5)按要求回答下列问题:
合成芳香炔化合物的方法之一是在催化条件下,含炔氢的分子与溴苯发生反应,如:

根据上式,请回答:
①丙能发生的反应是__________ (选填字母)。
a.取代反应 b.加成反应 c.水解反应 d.消去反应
②甲中含有的官能团名称为__________。
③符合下列条件的丙的同分异构体有__________种(不包括顺反异构)。
a分子中除苯环外不含其他环状结构;
b苯环上只有2个取代基,且其中一个是醛基。
【答案】C2H4 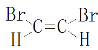 CH3CH=CHCH3+HCl
CH3CH=CHCH3+HCl![]() CH3CH2CHClCH3 2-甲基丁烷 c (醇)羟基 碳碳三键 24
CH3CH2CHClCH3 2-甲基丁烷 c (醇)羟基 碳碳三键 24
【解析】
(1)由二氧化碳和水的量先计算最简式,再结合相对分子质量计算分子式;
(2)顺-1,2-二溴乙烯中2个溴原子在同一侧;
(3)2-丁烯的结构简式为CH3CH=CHCH3,分子中含有碳碳双键,一定条件下能与HCl发生加成反应生成2—氯丁烷;
(4)![]() 的最长碳链含有4个碳原子,侧链为甲基;
的最长碳链含有4个碳原子,侧链为甲基;
(5)①丙的结构简式为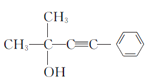 ,分子中含有羟基、碳碳三键和苯环;
,分子中含有羟基、碳碳三键和苯环;
②甲的结构简式为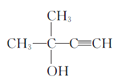 ,分子中含有(醇)羟基和碳碳三键;
,分子中含有(醇)羟基和碳碳三键;
③由丙的同分异构体分子中除苯环外不含其他环状结构,苯环上只有2个取代基,且其中一个是醛基可知,另一个取代基为四个C的丁烯烃基,判断丁烯烃基的数目,以及苯环上的相对位置可得。
(1)由在标准状况下,一定体积的该烃完全燃烧生成4.48LCO2和3.6g水可知,烃分子中C与H两种原子个数之比为![]() :
:![]() ×2=1:2,则该烃的最简式为CH2,最简式的式量是14,由相对分子质量是28可得烃的分子式为C2H4,故答案为:C2H4;
×2=1:2,则该烃的最简式为CH2,最简式的式量是14,由相对分子质量是28可得烃的分子式为C2H4,故答案为:C2H4;
(2)顺-1,2-二溴乙烯中2个溴原子在同一侧,结构式为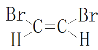 ,故答案为:
,故答案为: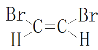 ;
;
(3)2-丁烯的结构简式为CH3CH=CHCH3,分子中含有碳碳双键,一定条件下能与HCl发生加成反应生成2—氯丁烷,反应的化学方程式为CH3CH=CHCH3+HCl![]() CH3CH2CHClCH3,故答案为:CH3CH=CHCH3+HCl
CH3CH2CHClCH3,故答案为:CH3CH=CHCH3+HCl![]() CH3CH2CHClCH3;
CH3CH2CHClCH3;
(4)![]() 的最长碳链含有4个碳原子,侧链为甲基,名称为2-甲基丁烷,故答案为:2-甲基丁烷;
的最长碳链含有4个碳原子,侧链为甲基,名称为2-甲基丁烷,故答案为:2-甲基丁烷;
(5)①丙的结构简式为 ,分子中含有羟基、碳碳三键和苯环,能发生取代反应、加成反应和消去反应,不能发生水解反应,故答案为:abd;
,分子中含有羟基、碳碳三键和苯环,能发生取代反应、加成反应和消去反应,不能发生水解反应,故答案为:abd;
②甲的结构简式为 ,分子中含有(醇)羟基和碳碳三键,故答案为:(醇)羟基和碳碳三键;
,分子中含有(醇)羟基和碳碳三键,故答案为:(醇)羟基和碳碳三键;
③由丙的同分异构体分子中除苯环外不含其他环状结构,苯环上只有2个取代基,且其中一个是醛基可知,另一个取代基为四个C的丁烯烃基,若烯烃为CH2=CH-CH2CH3,丁烯烃基有4种,若烯烃CH3CH=CHCH2,丁烯烃基有2种,若烯烃为CH2=C(CH3)2,丁烯烃基有2种,醛基和丁烯烃基在苯环上存在邻、间、对三种位置,则共有(4+2+2)×3=24种,故答案为:24。


科目:高中化学 来源: 题型:
【题目】已知N2(g)+3H2(g)![]() 2NH3(g)+Q1反应历程的能量变化如曲线I,说法正确的是
2NH3(g)+Q1反应历程的能量变化如曲线I,说法正确的是
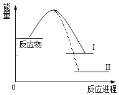
A.1molN≡N键能与3molH-H键能之和大于6molN-H键能,所以反应为放热
B.N2(g)+3H2(g)![]() 2NH3(l)+Q2反应历程的能量变化如曲线Ⅱ,则Q2>Q1
2NH3(l)+Q2反应历程的能量变化如曲线Ⅱ,则Q2>Q1
C.选择合适的催化剂,可以降低反应所需温度,Q1值也相应减少
D.2mol氨气的能量高于1mol氮气和3mol氢气的能量之和,所以反应需要高温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1-溴丁烷(密度1.2758 g/mL)是重要的有机合成中间体及有机溶剂,可以在实验室里用溴化钠、浓硫酸和1-丁醇为原料,经过如图六步制得。
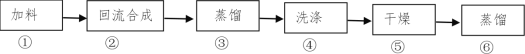
完成下列填空:
(1)通过步骤②获得粗产品,反应的化学方程式是___。此时产品往往呈红棕色,原因是____。实验室里有下列常用试剂,请根据实验需要为与步骤④相关的(2)(3)小题选择试剂,并用试剂编号填空:
a.NaOH溶液 b.NaHCO3溶液 c.NaHSO3 溶液 d.NaBr溶液
(2)产品的红棕色可用___除去(填写试剂编号),相应的离子方程式为___。
(3)选用浓硫酸洗去未反应的1-丁醇和有机副产物,然后除酸。最适宜的除酸试剂是__(填写试剂编号)。
(4)用浓硫酸(密度1.84g/mL)洗涤时,采用___(填写仪器名称)分离出___(填写“上”或“下”)层产物。
(5)检验产物中含有溴元素的实验方法是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为合成![]() 查阅资料得知一条合成路线:
查阅资料得知一条合成路线:
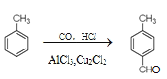
原料气CO的制备原理:HCOOH![]() CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。
(提示:甲酸(HCOOH)通常是一种无色易挥发的液体,它在浓硫酸作用下易分解)
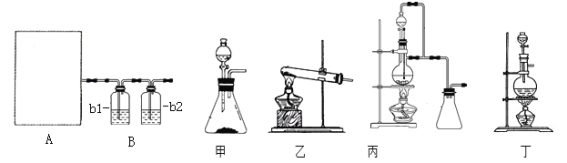
请完成下列问题:
(1)图A是利用甲酸制取CO的发生装置.根据实验原理,应选择图_____(填“甲”、“乙”、“丙”或“丁”);选择的理由是______________________。
(2)若用以上装置制备干燥纯净的CO,b1和b2中盛装的试剂分别是____________,_____。
(3)CO还可以和丙烯和氢气制取正丁醇,方程式如下:
CH3CH=CH2+CO+H2![]() CH3CH2CH2CHO
CH3CH2CH2CHO![]() CH3CH2CH2CH2OH;
CH3CH2CH2CH2OH;
在制取原料丙烯时,会产生少量SO2、CO2及水蒸气,某小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是_______(填序号)。
①2%品红溶液 ②溴水 ③石灰水 ④无水CuSO4 ⑤饱和Na2SO3溶液
(4)产物![]() 中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下:
中往往会混有少量甲苯,为了制取较纯净的产物,该小组对这两种有机物的物理性质进行了查阅,资料如下:
甲苯是无色透明液体,密度0.87,沸点:110.6℃,不溶于水,可混溶于苯等多数有机溶剂。无色或淡黄色透明液体,密度1.015,沸点204-205℃,微溶于水,易溶于醇、醚。通过这些资料,该小组设计了某些方法来进行产物的提纯,合理的是_________。
A 分液 B过滤 C蒸馏 D将甲苯氧化成苯甲酸再进行分液
(5)得到较纯净的产物之后,某位同学为了研究产物的化学性质,将产物和甲苯分别取样,并分别滴加溴水,发现溴水最终都褪色了,于是得出结论:产物和甲苯的化学性质相似。这位同学的结论是否正确?若不正确,请说明理由。_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镇痉药物C、化合物N以及高分子树脂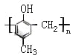 的合成路线如下:
的合成路线如下:

已知:RCHO
RCOOH RCOOR’
RCOOR’
(1)扁桃酸(![]() )有多种同分异构体,写出任意一种属于甲酸酯且含有亚甲基
)有多种同分异构体,写出任意一种属于甲酸酯且含有亚甲基![]() ,并且苯环上的一氯代物有两种的同分异构体的结构简式__________。
,并且苯环上的一氯代物有两种的同分异构体的结构简式__________。
(2)化合物M中官能团的名称是______,F和化合物M反应生成高分子树脂![]() 的反应类型是_____________。
的反应类型是_____________。
(3)酯类化合物C的分子式是C15H14O3 ,A在催化剂作用下可与H2 反应生成B,则扁桃酸和化合物B反应生成C的化学方程式为________________。
(4)N在NaOH溶液中发生水解反应的化学方程式是_____________。
(5)请写出由A的同系物制备比 ![]() 少2个氢原子芳香烃的合成路线。(无机物试剂任选)____________
少2个氢原子芳香烃的合成路线。(无机物试剂任选)____________
合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
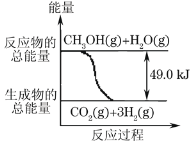
①CH3OH(g)+H2O(g)→CO2(g)+3H2(g) -49.0kJ
②CH3OH(g)+![]() O2(g)→CO2(g)+2H2(g)+192.9kJ
O2(g)→CO2(g)+2H2(g)+192.9kJ
下列说法正确的是( )
A.1molCH3OH完全燃烧放热192.9kJ
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+![]() O2(g)→CO2(g)+2H2(g)+Q的Q<192.9kJ
O2(g)→CO2(g)+2H2(g)+Q的Q<192.9kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.v(A)=0.5 mol·L-1·s-1B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1D.v(D)=1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于常温下的溶液,叙述正确的是( )
A.某氨水溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a<b
B.若1mL pH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11
C.在滴有酚酞溶液的氨水里,加入盐酸至恰好呈无色,则此时溶液的pH=7
D.1.0×10-6mol/L盐酸的pH=6,1.0×10-8mol/L盐酸的pH=8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某大理石(含Fe2O3)转化为氯化钙水合物储热材料和高纯度的碳酸钙,无论从经济效益还是资源综合利用都具有重要意义。其工艺流程示意图如下。
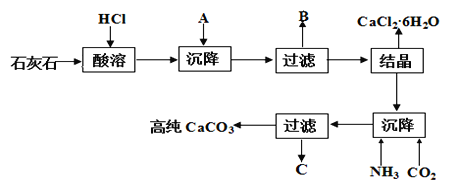
完成下列填空:
(1)上述流程中A是_________(填化学式,下同)、写出B中的成分___________。
(2)C可以作化肥,写出检验C中含有NH4+的方法:________。
(3)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是_____。
a 无毒
b 能导电
c 易溶于水
d 熔点较低(29℃熔化)
![]() CaCl2·6H2O
CaCl2·6H2O
(4)经过热重分析测得:CaCl2·6H2O在焙烧过程中,固体质量的减少值(纵坐标)随温度变化的曲线如图所示。则第一个相对稳定的物质的化学式是______。
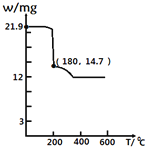
a CaCl2·4H2O
b CaCl2·2H2O
c CaCl2·H2O
d CaCl2
(5)工业还可以利用氨碱法的母液生产氯化钙。根据如图溶解度曲线,设计从含CaCl241%的饱和食盐水中,获得氯化钙水合物的流程______。
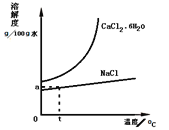
(流程示意:![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com