
��һ���������з�Ӧ��C6H5OH+CH3I �� C6H5OCH3 + HI
 +CH3CH2OH ��
+CH3CH2OH ��
������֬��һ������������ʹ�ù㷺�ľۺ���ϳɹ��̿ɱ�ʾ���£���Ӧ��������ȥ����

![]() ˫��A�루�����ȱ��飩��һ���������Ƶû�����֬��
˫��A�루�����ȱ��飩��һ���������Ƶû�����֬��
 ��1���������� ���������� ��ѡ����ţ�
��1���������� ���������� ��ѡ����ţ�
a������ b���ѻ� c���ѽ�
��2����Ӧ���� ����Ӧ���� ���Ӧ���ͣ���
��3����ɷ�Ӧ�۵Ļ�ѧ����ʽ�� ��
��4�������ɻ�����֬��ͬʱ���� ���ɡ�
��5��������֬���˵Ļ���������ijЩ���ʷ�Ӧ��ʹ�����������������������ʿ����� ������ţ� a���Ҵ� b���Ҷ��� c.1-����
��6�������ȱ����ж���ͬ���칹�壬��������������Ӧ���� �֣�д������һ�ֵ�ϵͳ���� ����˫��A�е�Hԭ�ӱ�1��Dԭ��ȡ������ȡ���IJ����� �֡�
��7����ҵ���ɱ���ȡ�����ж��ַ������磺

����һ��

��������
���������ڷ���һ֮���У� ����һ�㼴�ɣ���

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2009?�Ͼ���ģ����ҵ�Ͽ����úϳ�����CO��H2�Ļ�����壩�����״����練Ӧ�ܣ�����֪��
��2009?�Ͼ���ģ����ҵ�Ͽ����úϳ�����CO��H2�Ļ�����壩�����״����練Ӧ�ܣ�����֪��| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| ��� | ԭ�����и���ֵ�������� | |||
| CO | CO2 | H2 | N2 | |
| ��1�� | 19.7 | 0.0 | 59.1 | 21.2 |
| ��2�� | 20.7 | 0.3 | 62.1 | 16.9 |
| ��3�� | 16.9 | 1.3 | 50.7 | 31.1 |
| ��4�� | 19.8 | 5.5 | 59.4 | 15.3 |
| ��5�� | 20.3 | 10.9 | 60.9 | 7.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 A��B��C��D��E��FΪ��ѧ��ѧ�еij������ʣ�������A��1��2�ֶ�����Ԫ����ɣ���һ��������������ת����ϵ��������������⣺
A��B��C��D��E��FΪ��ѧ��ѧ�еij������ʣ�������A��1��2�ֶ�����Ԫ����ɣ���һ��������������ת����ϵ��������������⣺| 1 | 5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
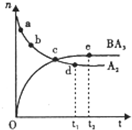 A��B��C��D��E��F����Ԫ�ط������������ڣ���ԭ��������������A��ԭ�������ڱ��а� ����С��A��D�����壬���γ����ӻ�����DA��C��Fͬ���壬���γ�FC2��FC3���ַ���B��D��E ���ߵ�����������Ӧ��ˮ��������֮����ɷ�Ӧ���ɿ������κ�ˮ���������о���CԪ �أ�����д���пհף�
A��B��C��D��E��F����Ԫ�ط������������ڣ���ԭ��������������A��ԭ�������ڱ��а� ����С��A��D�����壬���γ����ӻ�����DA��C��Fͬ���壬���γ�FC2��FC3���ַ���B��D��E ���ߵ�����������Ӧ��ˮ��������֮����ɷ�Ӧ���ɿ������κ�ˮ���������о���CԪ �أ�����д���пհף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010���Ϻ��б�ɽ�����������֡����������߿�ģ�⿼�� ���ͣ������
��һ���������з�Ӧ��C6H5OH +CH3I �� C6H5OCH3 + HI
 +CH3CH2OH ��
+CH3CH2OH ��
������֬��һ������������ʹ�ù㷺�ľۺ���ϳɹ��̿ɱ�ʾ���£���Ӧ��������ȥ����

 ˫��A�루�����ȱ��飩��һ���������Ƶû�����֬��
˫��A�루�����ȱ��飩��һ���������Ƶû�����֬��
 ��1���������� ���������� ��ѡ����ţ�
��1���������� ���������� ��ѡ����ţ�
a������ b���ѻ� c���ѽ�
��2����Ӧ���� ����Ӧ���� ���Ӧ���ͣ���
��3����ɷ�Ӧ�۵Ļ�ѧ����ʽ�� ��
��4�������ɻ�����֬��ͬʱ���� ���ɡ�
��5��������֬���˵Ļ���������ijЩ���ʷ�Ӧ��ʹ�����������������������ʿ����� ������ţ� a���Ҵ� b���Ҷ��� c.1-����
��6�������ȱ����ж���ͬ���칹�壬��������������Ӧ���� �֣�д������һ�ֵ�ϵͳ���� ����˫��A�е�Hԭ�ӱ�1��Dԭ��ȡ������ȡ���IJ����� �֡�
��7����ҵ���ɱ���ȡ�����ж��ַ������磺

����һ��

��������
���������ڷ���һ֮���У� ����һ�㼴�ɣ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com