
����Ŀ��ʵ��������NaOH ��������1.0mol/L��NaOH��Һ240mL��
��1��������Һʱ��һ����Է�Ϊ���¼������裺
�ٳ��� �ڼ��� ���ܽ� �ܵ�תҡ�� ��ת�� ��ϴ�� �߶��� ����ȴ
��ʵ������õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ�___��
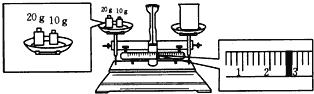
��2��ijͬѧ������һ������NaOH���壬������������ƽ�����ձ�����������ƽƽ����״̬��ͼ��ʾ���ձ���ʵ������Ϊ___g��Ҫ��ɱ�ʵ���ͬѧӦ�Ƴ�___gNaOH��
��3�������ƹ����У���������������ȷ�ģ����в���������Ũ��ƫ�ߵ���___��
��û��ϴ���ձ��Ͳ����� ��ת����Һʱ������������������ƿ����
������ƿ�����������������ˮ �ܶ���ʱ���ӿ̶���
���𰸡�250mL����ƿ 27.4 10.0g ��
��������
��1�����ݲ�����Ҫ��250mL����ƿ��
��2����ƽ��ƽ��ԭ������m��=m��+����������ѡȡ����ƿ���ݻ������������Ƶ�������
��3������![]() ����ʵ����
����ʵ����
��1�����ݲ�����Ҫ��250mL����ƿ�����Ա�ʵ������õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ�250mL����ƿ��
��2��m��=m��+�Σ���߷���30g�����룬���������2.6g������m�ձ�=30g-2.6g=27.4g��ѡȡ����ƿ���ݻ���250mL��m(NaOH)=cVM=1.0mol/L��0.25L��40g/mol=10.0g��
��3����û��ϴ���ձ��Ͳ����������ʵ����ʵ���ƫС��������ҺŨ��ƫ�ͣ��ʲ�ѡ����
��ת����Һʱ������������������ƿ���棬���ʵ����ʵ���ƫС��������ҺŨ��ƫ�ͣ��ʲ�ѡ����
���������ˮ����������ƿ�����������������ˮ��������ҺŨ����Ӱ�죬�ʲ�ѡ��
������ʱ���ӿ̶��ߣ���Һ���ƫС��������ҺŨ��ƫ�ߣ���ѡ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£�V L�Ȼ��⣨HCl���ܽ���1 Lˮ��(ˮ���ܶȽ���Ϊ1 g/mL)������Һ���ܶ�Ϊ�� g/mL����������Ϊw�����ʵ���Ũ��Ϊc mol/L�������й�ϵ�в���ȷ����( )
A. w=36.5c/1000�� B. c=1000��w/36.5
C. c=V��/(36.5V+22400) D. w=36.5V/(36.5V+22400)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���� ( )
A. AlCl3��Һ�еμӹ���NH3��H2O��Al3+ + 4OH-= AlO2-+ 2H2O
B. ����ˮ�ķ�Ӧ��Na+2 H2O =Na++2OH-+H2��
C. NaHSO4��Һ�м�BaCl2��Һ��SO42-+Ba2+=BaSO4��
D. ������ˮ�ķ�Ӧ��Cl2 + H2O = 2 H+ + ClO-+ Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£�35.5g�����������___L��������������ȫ���������Ȼ�������ʵ�����___mol�������ɵ������Ƴ�1L��Һ�����ʵ����ʵ���Ũ����___mol/L��������Һȡ��20mL������ˮϡ�ͳ�200mL��Һ����ϡϡ�����Һ�����ʵ����ʵ���Ũ����___mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����
A.�ð�ˮ���չ����Ķ�������![]()
B.̼�������ᷴӦ��![]()
C.FeS����ϡ���![]()
D.![]() ��Һ�����NaOH��Һ��
��Һ�����NaOH��Һ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�ã�п���̼��Ե��������������ҺΪ���Һ������ܷ�ӦʽΪ��Zn��s��+2MnO2��s��+H2O��l��![]() Zn��OH��2��s��+Mn2O3��s�� ����˵��������ǣ� ��
Zn��OH��2��s��+Mn2O3��s�� ����˵��������ǣ� ��
A. ��ع���ʱ��пʧȥ����
B. ��������ĵ缫��ӦʽΪ��2MnO2��s��+H2O��1��+2e��=Mn2O3��s��+2OH����aq��
C. ��ع���ʱ������������ͨ�����·����
D. ���·��ÿͨ��0.2mol���ӣ�п�����������ϼ�С6.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Dzⶨ���Ѿ���SO2�����ij��÷�������ԭ�����ڵ��������£��ù����Ĺ���������Һ��������Ʒ�лӷ�����SO2�����ü����Һ�ζ����ɵ��ᡣ
��ͼ��װ��װ�ã����װ�������ԣ���c��A��ע��20.00mL���Ѿƣ�10mL25%������Һ��C��D�зֱ�ע��20.00mL��5.00mLϡH2O2��Һ���ش��������⣺

��1��װ��B��������___________������ˮ��___________���a����b�����ڽ��롣
��2��C�з�����Ӧ�Ļ�ѧ����ʽΪ___________��ʹ��D��Ŀ����___________________��
��3����ձó������ʲ��˹��죬ԭ����______________________��
��4������ʮ���Ӻϲ�C��D�е���Һ������ָʾ������Ũ��Ϊc����λΪ![]() ����NaOH����Һ�ζ�������
����NaOH����Һ�ζ�������![]() ����ȡװ�ã���A��ע��20.00mL����ˮ����ͬ���ķ������հ�ʵ�飬����NaOH��Һ
����ȡװ�ã���A��ע��20.00mL����ˮ����ͬ���ķ������հ�ʵ�飬����NaOH��Һ![]() ��������Ѿ���SO2�ĺ���Ϊ___________mg/L������c��
��������Ѿ���SO2�ĺ���Ϊ___________mg/L������c��![]() ��
��![]() ��ʾ��
��ʾ��
��5�����Ѿ��к��е�SO2��������______________________������һ�㣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���� ZAX���γ�HmX���⻯���a g HmX ���� �� ��
A.![]() (A-Z+m)mol����B.
(A-Z+m)mol����B.![]() mol����
mol����
C.![]() (Z+m) mol����D.
(Z+m) mol����D.![]() mol HmX����
mol HmX����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����д���пհף�
��1������ 6.02��1023�� H ��H2O�������ʵ�����_______��1L 1 mol��L -1Na2SO4��Һ�� ����_____�� Na+��_____�� SO42- ��
��2��______mol H2O �к��е���ԭ������ 1.5 mol CO2�к��е���ԭ������ȡ�
��3���������ʵ����� NH3 �� CH4 ��ϣ���������� NH3 �� CH4 ������֮��Ϊ ______��
��4��Ҫʹ NH3�� CH4����ͬ��Ŀ��Hԭ�ӣ��� NH3�� CH4�����ʵ���֮��Ϊ_____��
��5����״���£��ܶ�Ϊ 0.75g��L -1�� NH3�� CH4 ��ɵĻ�������У�NH3���������Ϊ________���û�����������������ܶ�Ϊ________��
��6����֪ a g A �� b g B ǡ����ȫ��Ӧ���� 0.2 mol C �� d g D���� C ��Ħ������Ϊ ________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com