
| A. | BaO2的水解产物是Ba(OH)2和H2O2 | B. | PCl3水解的产物是HClO和PH3 | ||
| C. | CaC2水解的产物是Ca(OH)2和C2H2 | D. | Al2S3水解的产物是Al(OH)3和H2S |
分析 根据题意信息:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质,所以将物质分为阴离子和阳离子两部分,阳离子和氢氧根结合即为产物,阴离子和氢离子结合即为产物.
解答 解:水解是反应中各物质和水分别解离成两部分、然后两两重新组合成新的物质,该反应相当于复分解反应,反应过程中没有电子转移,其特征是没有元素化合价升降,
A.BaO2的水解产物是Ba(OH)2和H2O2,该反应中没有元素化合价升降,符合水解原理,故A不选;
B.该反应中Cl元素化合价由-1价变为+1价,有电子转移,不符合水解原理,故B选;
C、CaC2水解的产物是Ca(OH)2和C2H2,该反应中没有元素化合价升降,符合水解原理,故C不选;
D、Al2S3水解的产物是Al(OH)3和H2S,该反应中没有元素化合价升降,符合水解原理,故D不选;
故选B.
点评 本题考查了水解原理,正确理解题干信息是解本题关键,再结合元素化合价是否变化分析解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- | |
| B. | pH=1的溶液中大量存在Na+、NH4+、SiO32-、I- | |
| C. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- | |
| D. | 0.1mol•L-1NaAlO2溶液中可能大量存在Na+、H+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
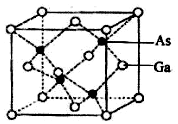 氮、磷、砷、钛的单质及其化合物在生产生活中有重要的应用.回答下列问题:
氮、磷、砷、钛的单质及其化合物在生产生活中有重要的应用.回答下列问题: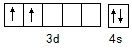 ,含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型为极性共价键、配位键,该配离子的配位数为6.
,含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2•H2O,其配离子中含有的化学键类型为极性共价键、配位键,该配离子的配位数为6.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在2L恒容密闭容器中,发生反应 2NO(g)+O2(g)?2NO2(g).
在2L恒容密闭容器中,发生反应 2NO(g)+O2(g)?2NO2(g).| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44% | B. | 54.22% | C. | 39.12% | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象或结论 |
| A | 将铁屑、溴水、苯混合加热 | 制取溴苯 |
| B | 先加入浓硫酸,再加入苯,最后滴入浓硝酸 | 制取硝基苯 |
| C | 向C6H5ONa溶液巾通入CO2气体 | 溶液出现浑浊,证明酸性:C6H5OH<H2CO3 |
| D | 乙醇和浓硫酸混合加热,将产生的气体通人酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色,证明乙醇发生消去反应生成乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水、氯化铁溶液 | B. | 溴水、酸性高锰酸钾溶液 | ||
| C. | 氯化铁溶液、碳酸钠溶液 | D. | 氯化铁溶液、酸性高锰酸钾溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com