
| A. | 硬水使肥皂去污能力减弱是因为发生了沉淀反应 | |
| B. | 用热的纯碱溶液可区别植物油和矿物油 | |
| C. | 从溴水中提取溴可用植物油作萃取剂 | |
| D. | 生产盐酸和人造脂肪必须用氢气作原料 |
分析 A.硬水中含大量的钙离子和镁离子;
B.植物油属于酯类,矿物油属于烃类;
C.植物油是由不饱和高级脂肪酸和甘油形成的酯;
D.盐酸是氢气和氯气制取,人造脂肪是不饱和脂肪酸加氢.
解答 解:A.硬水中含大量的钙离子和镁离子,能和肥皂中的硬脂酸根反应生成硬脂酸钙、硬脂酸镁沉淀,从而造成肥皂的浪费,故A正确;
B.植物油属于酯类,热的纯碱溶液能使其水解,而矿物油属于烃类,和纯碱不反应,故可以用热的纯碱溶液来鉴别,故B正确;
C.植物油是由不饱和高级脂肪酸和甘油形成的酯,结构中含碳碳双键,能和溴发生加成反应,故不能用植物油来萃取溴水中的溴,故C错误;
D.盐酸是氢气和氯气制取,人造脂肪是不饱和脂肪酸加氢,必须用氢气做原料,故D正确.
故选C.
点评 本题考查了油脂的结构和性质,难度不大,注意掌握植物油中含碳碳双键,而动物脂肪中没有.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 以下说法正确的是( )
以下说法正确的是( )| A. | ③④⑥ | B. | ①②③ | C. | ④⑤⑥ | D. | ①③④⑤⑥⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 s末氨气的反应速率=0.4 mol•(L•s)-1 | |
| B. | 前2 s时间内氢气的平均反应速率=0.9 mol•(L•s)-1 | |
| C. | 前4 s时间内氮气的平均反应速率=0.1mol•(L•s)-1 | |
| D. | 2~4 s时间内氨气的平均反应速率=0.2 mol•(L•s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2可用作呼吸面具供氧剂,它还可以用于消毒、杀菌和漂白 | |
| B. | NaH可用于和水反应制取氢气,NaH是共价化合物 | |
| C. | Na2CO3的水溶液可用于油污的去除,其热溶液去污效果更好 | |
| D. | 侯氏制碱法,首先制取的是NaHCO3,NaHCO3受热分解生成碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1mol/L•min | B. | 1.5mol/L•min | C. | 0.5mol/L•min | D. | 3mol/L•min |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 .写出A与溴水的反应方程式
.写出A与溴水的反应方程式 +3Br2→
+3Br2→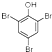 ↓+3HBr
↓+3HBr 或
或 (任写一个).
(任写一个). .
. 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com