
【题目】硝基苯是一种重要有机合成中间体,实验室可用如下反应合成:
C6H6+HNO3![]() C6H5—NO2+H2O ΔH<0
C6H5—NO2+H2O ΔH<0
已知:
①该反应在温度稍高的情况下会生成间二硝基苯。
②制备反应装置:

③有关数据如表:
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm3 | 溶解性 |
苯 | 5.5 | 80 | 0.88 | 微溶于水 |
硝基苯 | 5.7 | 211 | 1.205 | 难溶于水 |
间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
浓硝酸 | 83 | 1.4 | 易溶于水 | |
浓硫酸 | 338 | 1.84 | 易溶于水 |
请回答下列问题:
(1)合成硝基苯的反应类型为_____________。
(2)制备时需要配制25 mL的浓硝酸和x mL(0.552 mol)浓硫酸(98%)混合液,混合酸应该盛放在_____________中(填写仪器名称),x值为_____________。
(3)反应在50℃~60℃下进行,其主要原因可能是__________________________(写两点即可),常用的方法是__________________________。
(4)反应完毕所得的硝基苯中混有无机物杂质,需将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液、水洗涤并分液,第二次用水洗的目的是__________________________。
(5)进行分液的硝基苯中含有少许水分及有机物杂质,加入无水aCl2颗粒,静置片刻,然后倒入蒸馏烧瓶,弃去CaCl2,最后进行蒸馏纯化,蒸馏纯化的实验方案为__________________________。从实验安全角度考虑,在蒸馏纯化过程中,应选用空气冷凝管,不选用通水的直形冷凝管的原因是__________________________________。
(6)若反应开始时向仪器A中加入19.5 mL苯,反应完毕提纯后得到20 g硝基苯,则实验所得到的硝基苯产率为_____________(精确到0.1%)。
【答案】(1)取代反应
(2)分液漏斗 30
(3)防止温度过高浓硝酸分解、减少副产物间二硝基苯生成(或温度较低,反应速率慢,温度过高反应物转化率降低) 水浴加热
(4)洗去残留的NaOH及生成的盐
(5)首先控制蒸馏温度在80℃,收集该温度下的馏分,除去苯,然后控制蒸馏温度为211℃,收集该温度下的馏分,得到纯硝基苯 以免直形冷凝管通水冷却时温差过大而发生炸裂
(6)73.9%
【解析】(1)苯环上的H原子被—NO2取代生成硝基苯,所以该反应为取代反应。
(2)混合酸应该盛放在仪器B所示的分液漏斗中,通过分液漏斗来控制加入混酸的速率。![]() ,解得x=30。
,解得x=30。
(3)根据题目信息可知,合成硝基苯的反应为放热反应,从化学反应速率和化学平衡移动观点来解释温度控制,同时浓HNO3受热易分解生成NO2、温度较高时副产物间二硝基苯也易生成。由于温度低于100℃,所以可用水浴加热方法控制温度为50~60℃ 。
(4)先用水洗除去浓H2SO4、HNO3,再用稀NaOH溶液将剩余的少量酸转化为可溶性的盐,这些盐在蒸馏时不会变为气体,便于后续分离提纯硝基苯,最后水洗除去未反应的NaOH及生成的盐。
(5)硝基苯中含有未反应的苯、副产物间二硝基苯,由于三者沸点差异较大,故采用蒸馏方法提纯,首先应该在蒸馏温度80℃下蒸馏除去苯,然后再在211℃蒸馏得到硝基苯。
(6)25 mL浓HNO3物质的量=![]() ,20 mL苯物质的量=
,20 mL苯物质的量=![]() ,根据反应方程式可知,苯不足,生成的硝基苯应为0.22 mol,理论质量=0.22 mol×123 g/mol=27.06 g,实际质量为20 g,硝基苯的产率=
,根据反应方程式可知,苯不足,生成的硝基苯应为0.22 mol,理论质量=0.22 mol×123 g/mol=27.06 g,实际质量为20 g,硝基苯的产率=![]() 。
。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】下列电离方程式书写正确的是( )
A. NaHCO3═Na++H++CO32﹣ B. NaHSO4═Na++H++SO42﹣
C. Fe2(SO4)3═Fe3++SO42﹣ D. NH3H2O═NH4++OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【双流中学2017届下学期第二次适应性考试】某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl- + 2H+ = Cl2↑+ H2O。某学习小组拟探究该消毒液的变质情况。
(1)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过下列装置检验气体的成分可以判断消毒液是否变质。

学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙:______。
为了验证可能为甲,请完成下列实验方案。限选试剂:
A.98%的浓硫酸 B.1%的品红溶液 C.1.0 mol·L-1的KI-淀粉溶液
D.1.0 mol·L-1 的NaOH溶液 e.澄清石灰水 f.饱和NaCl溶液
所加试剂 | 预期现象和结论 |
试管A中加足量______(填序号); 试管B中加1%品红溶液; 试管C中加______(填序号)。 | 若A中________, B中________, C中________,则甲成立。 |
(2)用滴定法测定消毒液中NaClO的浓度。
①在使用滴定管之前首先进行的操作是_____________________;
②量取25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液v1 mL;(反应的化学方程式为:NaClO + Na2SO3 = NaCl+ Na2SO4)将b mol·L-1的用硫酸酸化的KMnO4溶液装入_________(填仪器名称)中;滴定剩余的Na2SO3溶液,反应的化学方程式为:_______________。当溶液由__________(填滴定终点现象)停止滴定,记录数据。
③重复上述滴定操作2次,平均消耗酸性KMnO4溶液v2 mL。则消毒液中NaClO的浓度___mol·L-1(用含a、b、v1、v2的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料。
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是________。
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O他们利用该反应设计如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O他们利用该反应设计如下制取氯气并验证其性质的实验。

回答下列问题:(1)该实验中A部分的装置是_______(填标号)。
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):_____________________________。
(3)写出D装置中发生反应的离子方程式_________________
(4)该实验存在明显的缺陷,请你提出改进的方法__________________________________________写出反应离子方程式_____________________________________。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取出25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol.L1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2===Na2S4O6+2NaI,共用去Na2S2O3溶液20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子核外电子排布的说法不正确的是 ( )。
A. 电子总是先排布在能量最低的电子层里
B. 每个电子层最多能容纳的电子数为2n2
C. 最外层电子数不超过8个(K为最外层时不超过2个)
D. S2-的M层电子数是K层电子数的3倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在任何条件下,纯水显中性,这是因为 ( )
A、PH=7 B、c(H+)=c(OH-)
C、c(H+)=c(OH-)=10-7mol/L D、c(H+)×c(OH-)=10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,对环境产生污染。为此,某化学兴趣小组设计了如下装置进行实验。玻璃管中①②③分别为CO检测试纸(浸有氯化钯溶液的滤纸,遇CO变黑色)、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
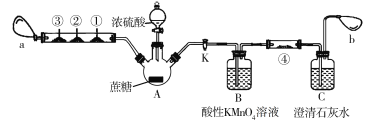
实验步骤如下:按图示连接好仪器,然后检查装置的气密性;装好试剂,夹紧止水夹K,向A瓶中的蔗糖上小心滴加浓硫酸,片刻后可观察到A瓶内蔗糖变黑,体积膨胀,有白雾产生,气球a鼓起,玻璃管中①号滤纸由白色变黑色,②号和③号滤纸均褪色。请回答以下问题:
(1)上图中盛装浓硫酸的仪器名称为________。待上述反应结束后,点燃酒精灯并在②号和③号滤纸的玻璃管附近均匀加热,观察到的现象是____________________。
(2)B瓶中酸性KMnO4溶液的作用是___________________________,发生反应的离子方程式为________________________________。
(3)打开止水夹K,使气球a内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊,但此现象并不能证明该反应生成了CO2。为了证明有CO2生成并简化实验装置,可在④号位置放上滴有__________的滤纸(从以下试剂中选择)。
A.品红溶液 B.酸性高锰酸钾溶液 C.溴水 D.澄清石灰水
(4)若反应生成的两种碳的氧化物在相同条件下的体积比为2∶1,则蔗糖炭化后体积膨胀发生反应的化学方程式可能为_______________________________。(若是氧化还原反应,请用单线桥法在化学方程式上标明电子转移的方向和数目。)
(5)若在尾端没有气球b,会有什么不良结果?______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com