
分析 (1)在反应达到平衡时由于产生C为1.2mol,根据方程式可知消耗的A、B的物质的量分别是0.6mol、1.2mol.因此平衡时各种物质的浓度是:c(A)=(2-0.6)mol÷2L=0.7mol/L;c(B)=(6-1.2)mol÷2L=2.4mol/L;c(C)=1.2mol÷2L=0.6mol/L,根据平衡常数的定义进行计算;
(2)在恒温恒容条件下,由于该反应是反应前后气体体积不等的反应,所以平衡混合气中C的体积分数仍为ω,则两平衡为完全等效平衡,即折算成一边的物质时,相关物质的物质的量相等,假设要加入B、C的物质的量分别是x、y,可以认为ymol的C不是加入的而是反应消耗A、B产生的,则根据方程式中的关系可知反应消耗A:y/2mol;B:ymol.则开始时加入的A为(1+y/2)mol;加入的B为(x+y)mol,所以1+y/2=2;x+y=6,据此答题.
解答 解:(1)在反应达到平衡时由于产生C为1.2mol,根据方程式可知消耗的A、B的物质的量分别是0.6mol、1.2mol.因此平衡时各种物质的浓度是:c(A)=(2-0.6)mol÷2L=0.7mol/L;c(B)=(6-1.2)mol÷2L=2.4mol/L;c(C)=1.2mol÷2L=0.6mol/L,所以该反应的平衡常数K$\frac{0.{6}^{2}}{0.7×2.{4}^{2}}$=0.0893,
故答案为:0.0893;
(2)在恒温恒容条件下,由于该反应是反应前后气体体积不等的反应,所以平衡混合气中C的体积分数仍为ω,则两平衡为完全等效平衡,即折算成一边的物质时,相关物质的物质的量相等,假设要加入B、C的物质的量分别是x、y,可以认为ymol的C不是加入的而是反应消耗A、B产生的,则根据方程式中的关系可知反应消耗A:y/2mol;B:ymol.则开始时加入的A为(1+y/2)mol;加入的B为(x+y)mol,所以1+y/2=2;x+y=6,解得x=4;y=2,即开始时加入1mol的A,4molB,2mol的C,
故答案为:4;2.
点评 本题主要考查了化学平衡常数的计算、恒温恒容条件下的等效平衡状态的判断及计算的知识,难度中等,注意等效平衡分完全等效和成比例等效,根据条件分析;


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2与O3 | B. | ${\;}_{6}^{14}$C与${\;}_{6}^{12}$C | ||
| C. | CH2Cl2与CHCl3 | D. | CH3-CH2-CH2-CH3与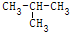 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Ca2+)、c(OH-)均增 | B. | c(Ca2+)、c(OH-)均保持不变 | ||
| C. | c(Ca2+)、c(OH-)均减小 | D. | 溶液质量增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 物质 | 杂质 | 所加试剂 | 分离方法 | 离子方程式 |
| 1. | NO | NO2 | |||
| 2. | Fe粉 | Al粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向0.1mol/L NaOH溶液滴加醋酸 | |
| B. | 向氢硫酸饱和溶液中通入氯气 | |
| C. | 向氯化铜溶液中加入适量氢氧化钡溶液 | |
| D. | 向硝酸银溶液通入氯化氢气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com