
”¾ĢāÄæ”æČēŗĪ½µµĶ“óĘųÖŠ![]() µÄŗ¬Įæ¼°ÓŠŠ§µŲæŖ·¢ĄūÓĆ
µÄŗ¬Įæ¼°ÓŠŠ§µŲæŖ·¢ĄūÓĆ![]() ŅżĘšĮĖČ«ŹĄ½ēµÄĘÕ±éÖŲŹÓ”£ÄæĒ°¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØŹĒÓĆ
ŅżĘšĮĖČ«ŹĄ½ēµÄĘÕ±éÖŲŹÓ”£ÄæĒ°¹¤ŅµÉĻÓŠŅ»ÖÖ·½·ØŹĒÓĆ![]() Ą“Éś²śČ¼ĮĻ¼×“¼”£ĪŖĢ½¾æøĆ·“Ó¦ŌĄķ£¬½ųŠŠČēĻĀŹµŃé£ŗŌŚČŻ»żĪŖ1LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė
Ą“Éś²śČ¼ĮĻ¼×“¼”£ĪŖĢ½¾æøĆ·“Ó¦ŌĄķ£¬½ųŠŠČēĻĀŹµŃé£ŗŌŚČŻ»żĪŖ1LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė![]() ŗĶ
ŗĶ![]() £¬ŌŚ
£¬ŌŚ![]() ĻĀ·¢Éś·¢Ó¦
ĻĀ·¢Éś·¢Ó¦![]() ŹµŃé²āµĆ
ŹµŃé²āµĆ![]() ŗĶ
ŗĶ![]() µÄĪļÖŹµÄĮæ
µÄĪļÖŹµÄĮæ![]() Ėꏱ¼ä±ä»ÆČēĶ¼1ĖłŹ¾£ŗ
Ėꏱ¼ä±ä»ÆČēĶ¼1ĖłŹ¾£ŗ
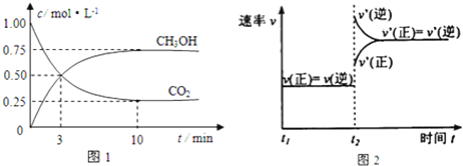
£Ø1£©ĻĀĮŠŹĀŹµÄÜĖµĆ÷·“Ó¦µ½“ļĘ½ŗāדĢ¬µÄŹĒ______________
A.ČŻĘ÷ÄŚµÄĆÜ¶Č²»ŌŁøıä B. CO2ŗĶH2 µÄĪļÖŹµÄĮæ±Č²»ŌŁøıä
C.vÕż£ØCO2£©=3vÄę£ØH2£© D. ČŻĘ÷ÄŚµÄŃ¹Ēæ²»ŌŁøıä
£Ø2£©![]() “ļĘ½ŗāŹ±£¬
“ļĘ½ŗāŹ±£¬![]() µÄĢå»ż·ÖŹżĪŖ____________£¬Ę½ŗā³£ŹżĪŖ______
µÄĢå»ż·ÖŹżĪŖ____________£¬Ę½ŗā³£ŹżĪŖ______![]() ±£ĮōĮ½Ī»Š”Źż
±£ĮōĮ½Ī»Š”Źż![]() £»øĆĪĀ¶ČĻĀ£¬²āµĆijŹ±æĢ£¬
£»øĆĪĀ¶ČĻĀ£¬²āµĆijŹ±æĢ£¬![]() ”¢
Ӣ![]() Ӣ
”¢![]() ŗĶ
ŗĶ![]() µÄÅØ¶Č¾ł
µÄÅØ¶Č¾ł![]() £¬Ōņ“Ė Ź±
£¬Ōņ“Ė Ź±![]() Õż
Õż![]() ______
______![]() Äę
Äę![]() Ģī”°
Ģī”°![]() ”±”°
”±”°![]() ”±»ņ”°
”±»ņ”°![]() ”±
ӱ![]() ӣ
ӣ
£Ø3£©ÓÉĶ¼2æÉÖŖ£¬µ±ĪĀ¶ČÉżøßµ½![]() “ļĘ½ŗāŹ±£¬KÖµ__________
“ļĘ½ŗāŹ±£¬KÖµ__________![]() Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±
Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±![]() ”£
ӣ
£Ø4£©ĻĀĮŠ“ėŹ©ÖŠ²»ÄÜŹ¹![]() µÄ×Ŗ»ÆĀŹŌö“óµÄŹĒ______”£
µÄ×Ŗ»ÆĀŹŌö“óµÄŹĒ______”£
A.ŌŚŌČŻĘ÷ÖŠŌŁ³äČė1mol![]()
B.ŌŚŌČŻĘ÷ÖŠŌŁ³äČė![]()
C.ĖõŠ”ČŻĘ÷µÄČŻ»ż
![]() Ź¹ÓĆøüÓŠŠ§µÄ“߻ƼĮ
Ź¹ÓĆøüÓŠŠ§µÄ“߻ƼĮ
E.½«Ė®ÕōĘų“ÓĢåĻµÖŠ·ÖĄė³ö
F.ŌŚŌČŻĘ÷ÖŠ³äČė1molHe
”¾“š°ø”æD ![]() 5.33 > ¼õŠ” BDF
5.33 > ¼õŠ” BDF
”¾½āĪö”æ
¢ÅÖŠAŃ”Ļī£¬øł¾ŻĆÜ¶Č¹«Ź½![]() £¬ĘųĢåÖŹĮæƻӊ±ä»Æ£¬ČŻĘ÷Ģå»żĆ»ÓŠ±ä»Æ£¬¼“Ćܶȏ¼ÖÕƻӊøı䣬Ņņ“Ė²»ÄÜ×÷ĪŖÅŠ¶ĻĘ½ŗāµÄ±źÖ¾£¬¹ŹA“ķĪó£»
£¬ĘųĢåÖŹĮæƻӊ±ä»Æ£¬ČŻĘ÷Ģå»żĆ»ÓŠ±ä»Æ£¬¼“Ćܶȏ¼ÖÕƻӊøı䣬Ņņ“Ė²»ÄÜ×÷ĪŖÅŠ¶ĻĘ½ŗāµÄ±źÖ¾£¬¹ŹA“ķĪó£»
BŃ”Ļī£¬CO2ŗĶH2æŖŹ¼±ČŹĒ1:3£¬ŌŚÕūøö·“Ó¦¹ż³ĢÖŠĻūŗÄŅ²ŹĒ°“ÕÕ1:3ŌŚĻūŗÄ£¬Ņņ“ĖŌŚ·“Ó¦¹ż³ĢÖŠŹ£ÓąµÄCO2ŗĶH2µÄĪļÖŹµÄĮæ±ČŹ¼ÖÕĪ“1:3£¬Ņņ“Ė²»ÄÜ×÷ĪŖÅŠ¶ĻĘ½ŗāµÄ±źÖ¾£¬¹ŹB“ķĪó£»
CŃ”Ļī£¬vÕż(CO2)£¬·“Ó¦Õż·½Ļņ£¬vÄę(H2)£¬·“Ó¦Äę·½Ļņ£¬Į½øö²»Ķ¬µÄ·½Ļņ£¬»¹ŅŖ×ńŃĖŁĀŹ±ČµČÓŚ¼ĘĮæĻµŹżÖ®±Č£¬Ó¦øĆ3vÕż(CO2) = vÄę(H2)£¬¹ŹC“ķĪó£»
DŃ”Ļī£¬øĆ·“Ó¦ĪŖ²»µČĢå»ż·“Ó¦£¬Ņņ“ĖÕżĻņ·“Ó¦Ź±£¬ČŻĘ÷ÄŚµÄŃ¹ĒæŌŚ²»¶Ļ¼õŠ”£¬µ±Ń¹Ēæ²»ŌŁøı䏱¾Ķ“ļµ½Ę½ŗā£¬¹ŹDÕżČ·£»
×ŪÉĻĖłŹö£¬“š°øD”£
¢Ęøł¾Ż·“Ó¦¼°Ķ¼Ļń·ÖĪö£¬ĄūÓĆ”°Čż²½×ß”±Ė¼Ļė
CO2(g) £« 3H2(g) ![]() CH3OH (g) £« H2O(g)
CH3OH (g) £« H2O(g)
æŖŹ¼ 1 mol”¤L-1 3 mol”¤L-1 0 0
×Ŗ»Æ 0.75 mol”¤L-1 2.25 mol”¤L-1 0.75 mol”¤L-1 0.75 mol”¤L-1
Ę½ŗā 0.25 mol”¤L-1 0.75 mol”¤L-1 0.75 mol”¤L-1 0.75 mol”¤L-1
![]()
¹ŹµŚŅ»æÕ“š°øĪŖ30%£»
øł¾ŻĘ½ŗā³£Źż¹«Ź½“śČė
![]()
¹ŹµŚ¶žæÕ“š°øĪŖ5.33£»
øł¾ŻÅضČÉĢ¹«Ź½“śČėµĆ³öŹż¾ŻÓė»ÆŃ§Ę½ŗā³£Źż±Č½Ļ
![]()
ÅضČÉĢŠ”ÓŚĘ½ŗā³£Źż£¬¼“ŅŖ±ä“ó£¬ŌņÉś³ÉĪļŅŖŌö¼Ó£¬Ę½ŗāÕżĻņŅĘ¶Æ¼“Õż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¹ŹµŚČżæÕ“š°øĪŖ”°>”±£»
¢Ēøł¾ŻĶ¼ĻóÖŖ£¬ÉżøßĪĀ¶Č£¬Äę·“Ó¦ĖŁĀŹ“óÓŚÕż·“Ó¦ĖŁĀŹ£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬KÖµ¼õŠ”£¬¹Ź“š°øĪŖ¼õŠ”£»
¢ČAŃ”Ļī£¬ŌŚŌČŻĘ÷ÖŠŌŁ³äČė1molĒāĘų£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¶žŃõ»ÆĢ¼ĻūŗÄ£¬¶žŃõ»ÆĢ¼µÄ×Ŗ»ÆĀŹŌö“󣬹ŹAÄÜŌö“ó×Ŗ»ÆĀŹ£»
BŃ”Ļī£¬ŌŚŌČŻĘ÷ÖŠŌŁ³äČė1 mol ¶žŃõ»ÆĢ¼£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬ĖäČ»¶žŃõ»ÆĢ¼ÓÖĻūŗÄĮĖ£¬øł¾Ż×Ŗ»ÆĀŹ¹«Ź½æÉÖŖ£¬·Ö×Ó·ÖÄø¶¼±ä“ó£¬ÓÉÓŚĘ½ŗāŅĘ¶ÆŹĒĪ¢ČõµÄ£¬Ņņ“Ė·Ö×ÓŌö¼Ó·ł¶ČŠ”ÓŚ·ÖÄøŌö¼ÓµÄ·ł¶Č£¬×Ŗ»ÆĀŹ¼õŠ”£¬¹ŹB²»ÄÜŌö“ó×Ŗ»ÆĀŹ£»
CŃ”Ļī£¬ĖõŠ”ČŻĘ÷µÄČŻ»ż£¬Ń¹ĒæŌö“ó£¬Ę½ŗāĻņĢå»ż¼õŠ”µÄ·½ĻņŅĘ¶Æ¼“ÕżĻņŅĘ¶Æ£¬×Ŗ»ÆĀŹ±ä“󣬹ŹCÄÜŌö“ó×Ŗ»ÆĀŹ£»
DŃ”Ļī£¬Ź¹ÓĆøüÓŠŠ§µÄ“߻ƼĮ£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬µ«Ę½ŗāƻӊ·¢ÉśŅĘ¶Æ£¬×Ŗ»ÆĀŹ²»±ä£¬¹ŹD²»ÄÜŌö“ó×Ŗ»ÆĀŹ£»
EŃ”Ļī£¬½«Ė®ÕōĘų“ÓĢåĻµÖŠ·ÖĄė³ö¼“¼õŠ”Éś³ÉĪļÅØ¶Č£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬×Ŗ»ÆĀŹŌö“󣬹ŹEÄÜŌö“ó×Ŗ»ÆĀŹ£»
FŃ”Ļī£¬ŌŚŌČŻĘ÷ÖŠ³äČė1molHe£¬ĢåĻµŃ¹ĒæŌö“󣬵«·“Ó¦ÅضČƻӊ·¢ÉśøÄ±ä£¬Ę½ŗā²»ŅĘ¶Æ£¬×Ŗ»ÆĀŹ²»±ä£»¹ŹF²»ÄÜŌö“ó×Ŗ»ÆĀŹ£»
×ŪÉĻĖłŹö£¬ÕżČ·“š°øĪŖBDF



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬½«Ņ»¶ØĮæµÄ¹ĢĢå A ÖĆÓŚ¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·Ö½ā·“Ó¦£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗāA(s) ![]() 2B(g)+C(g)£¬ŅŌĻĀæÉŅŌ×÷ĪŖĘ½ŗā±źÖ¾µÄŹĒ
2B(g)+C(g)£¬ŅŌĻĀæÉŅŌ×÷ĪŖĘ½ŗā±źÖ¾µÄŹĒ
A.2vÕż(B)=vÄę(C)
B.ĘųĢå B µÄĢå»ż·ÖŹż²»±ä
C.»ģŗĻĘųĢåµÄĘ½¾łÄ¦¶ūÖŹĮæ²»±ä
D.»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓƵēŹÆÖʱøµÄŅŅČ²ĘųĢåÖŠ³£»ģÓŠÉŁĮæH2SĘųĢ唣ĒėÓĆĶ¼ÖŠŅĒĘ÷ŗĶŅ©Ę·×é³ÉŅ»Ģ×Öʱø”¢¾»»ÆŅŅČ²µÄ×°ÖĆ£¬²¢æÉĶعż²ā¶ØŅŅČ²µÄĮ棬“Ó¶ų¼ĘĖćµēŹÆ“æ¶Č”£
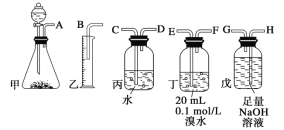
(1)µēŹÆÖʱøµÄŅŅČ²ĘųĢå·½³ĢŹ½______________________________£»
(2)½ųŠŠŹµŃ鏱£¬ĖłÖĘĘųĢå“Ó×óĻņÓŅĮ÷£¬ŅĒĘ÷µÄÕżČ·Į¬½ÓĖ³ŠņŹĒ________________(Ģī½ÓæŚ×ÖÄø)£»
(3)ĪŖĮĖŹ¹ŹµŃéÖŠĘųĮ÷Ę½ĪČ£¬¼×ÖŠ·ÖŅŗĀ©¶·ĄļµÄŅŗĢåXĶس£ÓĆ__________£»
(4)ČōŌŚ±ź×¼×“æöĻĀäåĖ®ÓėŅŅČ²ĶźČ«·“Ӧɜ³ÉC2H2Br4£¬ŅŃÖŖ³ĘČ”µēŹÆm g£¬²āµĆĮæĶ²ÄŚŅŗĢåĢå»żV mL£¬ŌņµēŹÆ“æ¶ČæɱķŹ¾ĪŖ_________________________£»
(5)Čōƻӊ³żH2SµÄ×°ÖĆ£¬²ā¶Ø½į¹ū½«»į____(Ģī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°²»±ä”±) £¬ĄķÓÉŹĒ£Ø·½³ĢŹ½±ķŹ¾£©_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆĻĀĶ¼×°ÖĆ£¬æÉŅŌÄ£ÄāĢśµÄµē»Æѧ·Ą»¤”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A. ČōXĪŖĢ¼°ō£¬ĪŖ¼õ»ŗĢśµÄøÆŹ“£¬æŖ¹ŲKÓ¦øĆÖĆÓŚM“¦
B. ČōXĪŖŠæ£¬æŖ¹ŲKÖĆÓŚM“¦£¬øƵē»Æѧ·Ą»¤·Ø³ĘĪŖĪžÉüŃō¼«µÄŅõ¼«±£»¤·Ø
C. ČōXĪŖĢ¼°ō£¬KÓėMĮ¬½ÓŹ±£¬Ņ»¶ĪŹ±¼äŗóČÜŅŗµÄpH¼õŠ”
D. ČōXĪŖŠæ£¬KÓėNĮ¬½ÓŹ±£¬Xµē¼«²śÉśĘųÅŻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A.0.1 mol µÄ11BÖŠ£¬Ėłŗ¬ÖŠ×ÓŹżĪŖ0.6NA
B.±ź×¼×“æöĻĀ£¬22.4 L CCl4ÖŠĖłŗ¬ĀČŌ×ÓŹżĪŖ4NA
C.1.0 mol CH4Óė1.0 molCl2ŌŚ¹āÕÕĻĀ·“Ӧɜ³ÉµÄCH3Cl·Ö×ÓŹżĪŖ1.0NA
D.³£ĪĀ³£Ń¹ĻĀ£¬124 g P4ÖŠĖłŗ¬P”ŖP¼üŹżÄæĪŖ4NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾Żµē»ÆѧÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā”£
¢ń”¢Ä³Š”×éĶ¬Ń§ÉčĻėÓĆČēĶ¼×°ÖƵē½āĮņĖį¼ŲČÜŅŗĄ“ÖĘČ”ŃõĘų”¢ĒāĘų”¢ĮņĖįŗĶĒāŃõ»Æ¼Ų”£
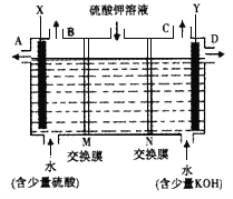
(1)X¼«ÓėµēŌ“µÄ_____£ØĢīÕż»ņøŗ£©¼«ĻąĮ¬£¬ĒāĘų“Ó____ £ØŃ”ĢīA”¢ B”¢C»ņD£©æŚµ¼³ö”£
(2)Ąė×Ó½»»»Ä¤Ö»ŌŹŠķŅ»ĄąĄė×ÓĶعż£¬ŌņMĪŖ________£ØĢīŅõĄė×Ó»ņŃōĄė×Ó£¬ĻĀĶ¬£©½»»»Ä¤£¬NĪŖ________½»»»Ä¤”£
(3)Čō½«ÖʵƵÄĒāĘų”¢ŃõĘųŗĶĒāŃõ»Æ¼ŲČÜŅŗ×éŗĻĪŖĒāŃõČ¼ĮĻµē³Ų£ØŹÆÄ«ĪŖµē¼«£©£¬Ōņµē³ŲÕż¼«µÄµē¼«·“Ó¦Ź½ĪŖ___________________
¢ņ”¢Ē¦Šīµē³ŲŹĒ³£¼ūµÄ¶ž“Īµē³Ų£¬Ęä·Åµē·“Ó¦ŗĶ³äµē·“Ó¦±ķŹ¾ČēĻĀ£ŗPb(s)£«PbO2(s)£«2H2SO4(aq)![]() 2PbSO4(s)£«2H2O(l)
2PbSO4(s)£«2H2O(l)
Š“³öĖü·ÅµēŹ±Õż¼«µÄµē¼«·“Ó¦Ź½______________________________________£»
³äµēŹ±Ņõ¼«µÄµē¼«·“Ó¦Ź½______________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖŠčÉč¼ĘŅ»Ģ׏µŃé×°ÖĆĄ“µē½ā±„ŗĶŹ³ŃĪĖ®£¬²¢²āĮæµē½ā²śÉśµÄĒāĘųµÄĢå»ż(Ō¼6 mL)ŗĶ¼ģŃéĀČĘųµÄŃõ»ÆŠŌ(²»Ó¦½«¶ąÓąµÄĀČĘųÅÅČėæÕĘųÖŠ)”£
(1)ŹŌ“ÓĻĀĶ¼ÖŠŃ”ÓĆ¼øÖÖ±ŲŅŖµÄŅĒĘ÷£¬Į¬³ÉŅ»ÕūĢ××°ÖĆ£¬ø÷ÖÖŅĒĘ÷½ÓæŚµÄĮ¬½ÓĖ³Šņ(Ģī±ąŗÅ)ŹĒA½Ó__________£¬B½Ó__________”£
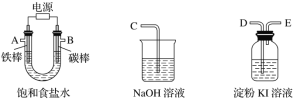
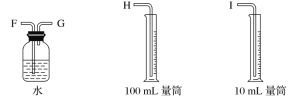
(2)Ģś°ō½ÓÖ±Į÷µēŌ“µÄ________¼«£»Ģ¼°ōÉĻ·¢ÉśµÄµē¼«·“Ó¦ĪŖ_______”£
(3)ÄÜĖµĆ÷ĀČĘų¾ßÓŠŃõ»ÆŠŌµÄŹµŃéĻÖĻóŹĒ_______________________”£
(4)¼Ł¶Ø×°ČėµÄŹ³ŃĪĖ®ĪŖ50 mL£¬Ņ»¶ĪŹ±¼äŗ󣬲śÉś5.6 mL(±ź×¼×“æö)H2Ź±£¬ĖłµĆČÜŅŗŌŚ25 ”ꏱµÄpH£½________”£
(5)Čō½«Bµē¼«»»³ÉĢśµē¼«£¬Š“³öŌŚµē½ā¹ż³ĢÖŠUŠĪ¹Üµ×²æ³öĻÖµÄĻÖĻó£ŗ __________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķøų³öĘßÖÖŌŖĖŲµÄĻą¹ŲŠÅĻ¢£¬øł¾ŻŅŌĻĀŠÅĻ¢ĢīæÕ£ŗ
ŌŖĖŲ | Ļą¹ŲŠÅĻ¢ |
A | ŗĖĶāµē×ÓŹżŗĶµē×Ó²ćŹżĻąµČ |
B | »łĢ¬Ō×Ó2pÄܼ¶ÓŠ3øöĪ“³É¶Ōµē×Ó |
C | ŌŚµŲæĒÖŠŗ¬Įæ×īøß |
D | ÄæĒ°£¬ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµēøŗŠŌ×ī“ó |
E | »łĢ¬Ō×ÓŗĖĶāµē×Ó·Ö“¦6øö²»Ķ¬Äܼ¶£¬ĒŅĆæøöÄܼ¶¾łŅŃÅÅĀś |
F | Ō×ÓŠņŹżµČÓŚDÓėEµÄŌ×ÓŠņŹżÖ®ŗĶ |
G | »łĢ¬Ō×Ó2pÄܼ¶ÉĻÓŠĮ½øöæÕ¹ģµĄ |
(1)Š“³öDŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆ___________________”£
(2)14gBµÄµ„ÖŹ·Ö×ÓÖŠ¦Š¼üµÄøöŹżĪŖ____________”£
(3)CŌŖĖŲµÄĒā»ÆĪļµÄ·ŠµćŹĒĶ¬×åŌŖĖŲĒā»ÆĪļÖŠ×īøߵģ¬ŌŅņŹĒ________”£
(4)B”¢C”¢D 3ÖÖŌŖĖŲµÄµēøŗŠŌÓɓ󵽊”µÄĖ³ŠņĪŖ________(ÓĆŌŖĖŲ·ūŗűķŹ¾)”£
(5)Š“³öŅ»ÖÖÓėB2»„ĪŖµČµē×ÓĢåµÄ·Ö×Ó»ņĄė×Ó____________”£
(6)ŅŃÖŖBA5ĪŖĄė×Ó»ÆŗĻĪļ£¬Š“³öĘäµē×ÓŹ½£ŗ_______”£
(7)µŚ¶žÖÜĘŚÖŠ£¬µŚŅ»µēĄėÄܽéÓŚBŌŖĖŲŗĶG ŌŖĖŲ¼äµÄŌŖĖŲĪŖ ____(Ģī”°ŌŖĖŲ·ūŗÅ”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z×é³ÉµÄ»ÆŗĻĪļY2XŗĶZX2”£Y2XČÜÓŚĖ®ŠĪ³ÉµÄČÜŅŗÄÜÓėZX2·“Ӧɜ³ÉŅ»ÖÖ»ÆŗĻĪļY2ZX3”£ŅŃÖŖČżÖÖŌŖĖŲŌ×ÓµÄÖŹ×Ó×ÜŹżĪŖ25£¬ĒŅZŗĶYµÄŌ×ÓŠņŹżÖ®ŗĶ±ČXµÄŌ×ÓŠņŹż2±¶»¹¶ą1£¬ZŌ×ÓÓŠ2øöµē×Ó²ć£¬×īĶā²ćµē×ÓŹżŹĒŗĖĶāµē×ÓŹżµÄ2/3±¶£¬ŹŌ»Ų“š£ŗ
£Ø1£©XŌŖĖŲµÄĆū³Ę£ŗX____£¬YŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆ____£¬ZŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼_______”£
£Ø2£©ÓƵē×ÓŹ½±ķŹ¾ZX2µÄŠĪ³É¹ż³Ģ_____”£
£Ø3£©Y2X¶ŌÓ¦Ė®»ÆĪļµÄµē×ÓŹ½_____£¬ĘäÖŠ“ęŌŚµÄ»Æѧ¼üÓŠ_____”£
£Ø4£©Š“³öY2XČÜÓŚĖ®µÄČÜŅŗÓėZX2·“Ó¦µÄ»Æѧ·½³ĢŹ½_______”£
£Ø5£©XµÄĒā»ÆĪļ±ČĶ¬Ö÷×åµÄĒā»ÆĪļµÄČŪ·ŠµćĆ÷ĻŌĘ«øßµÄŌŅņ____”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com