
| ʵ �� �� | ���� | ���� |
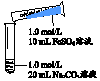 | 1����Ϻ���ְ�ɫ��״�����������ֳ����ʻ���ɫ�������ݲ��� 2������5-8���ӣ�����ɫ���������࣬���ձ�ɺ��ɫ |
| ʵ��� | ���� | ���� |
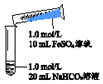 | 1����Ϻ��Թ��г��ְ�ɫ����״���ǣ�Ƭ�̺��д������ݲ��� 2����ճ�����Թ��ڱڵİ�ɫ����״���DZ����ɫ����Խ��Խ�ࣻ20���Ӻ�ɫ�������Գ��� |
| ʵ��� | ���� | ���� |
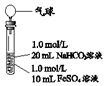 | 1����Ϻ��Թ��г��ְ�ɫ����״���ǣ�Ƭ�̺��д������ݲ��� 2��һ��ʱ����������ž��������Ľ��������Թܣ������5Сʱ���������ͣ��Թ��г�����ʼ�ձ��ְ�ɫ |
���� ��1��������������̼�����������FeCO3��
������������̼���ƻ���а�ɫ��״����������������ɻ���ɫ������ɺ��ɫ������Ϊ����������������Ϊ����������
�۷�Ӧδ���������������������ӱ�������
��2����NaHCO3�д��ڵ���ƽ�⣺HCO3-?H++CO32-����FeSO4��Ӱ���ƽ�⣬�ݴ˷�����
��FeCO3��ϡ���ᷴӦ�ж�����̼���ɣ��Ƚϲ�������Ķ��ٿ�֪��FeCO3������Դ�С��
��3��Ϊ��ֹ����FeCO3��¶�ڿ����л����������ɺ���ɫ��ˮ�����������ų�װ�õĿ�����
��4��a����ʵ��I��֪̼�����Ʊ���FeCO3���ȵͣ�NaHCO3��Һ���������Ƶ�FeCO3���ȸߣ�
b����1L 1.0mol/L NaHCO3������FeSO4��Һ��Ӧ�ж�����̼���ɣ������Ͽ��Ʊ�FeCO3����116g��
c��ʪƷFeCO3�ڿ����л�����������ˮ��������FeO��OH��������ʽΪ 4FeCO3+O2+2H2O=4FeO��OH��+4CO2��
d����ҵ����NH4HCO3��FeSO4��Ӧ���Ʊ����ȸ��ߵ�FeCO3��
��� �⣺��1��������������̼�����������FeCO3�����ӷ���ʽΪ��Fe2++CO32-=FeCO3����
�ʴ�Ϊ��Fe2++CO32-=FeCO3����
������������̼���ƻ���а�ɫ��״����������������ɻ���ɫ������ɺ��ɫ������Ϊ����������������Ϊ����������
�ʴ�Ϊ����ɫ��״��ɻ���ɫ������ɺ��ɫ��
�۷�Ӧδ���������������������ӱ����������������ӣ��ʽ�����������Fe3+��Fe2+��
�ʴ�Ϊ��Fe3+��Fe2+��
��2����NaHCO3�д��ڵ���ƽ�⣺HCO3-?H++CO32-����FeSO4��Fe2++CO32-=FeCO3����ƽ�����ƣ�H++HCO3-=CO2��+H2O���ʲ����������ݣ�
�ʴ�Ϊ��NaHCO3�д��ڵ���ƽ�⣺HCO3-?H++CO32-����FeSO4��Fe2++CO32-=FeCO3����ƽ�����ƣ�H++HCO3-=CO2��+H2O��
��FeCO3��ϡ���ᷴӦ�ж�����̼���ɣ��Ƚϲ�������Ķ��ٿ�֪��FeCO3������Դ�С����ֱ����ֳ������Ĺ��ˡ�ϴ�ӡ�������ȡ�����������ֹ��壬������ϡ����������ܽ⣬ʵ����в����������ʵ����в���������࣬˵��ʵ������ù�����FeCO3�ĺ�����ʵ���ࣻ
�ʴ�Ϊ��������ϡ����������ܽ⣬ʵ����в����������ʵ����в���������ࣻ
��3�������֪��ʪ���FeCO3��¶�ڿ����л����������ɺ���ɫ��ˮ������������ʵ��III���÷�Ӧ�ų�CO2������Ӧ������O2�Ļ�����
�ʴ�Ϊ����Ӧ�ų�CO2������Ӧ������O2�Ļ�����
��4��a����ʵ��I��֪̼�����Ʊ���FeCO3���ȵͣ�NaHCO3��Һ���������Ƶ�FeCO3���ȸߣ�����ȷ��
b����1L 1.0mol/L NaHCO3������FeSO4��Һ��Ӧ�ж�����̼���ɣ������Ͽ��Ʊ�FeCO3����116g���ʴ���
c��ʪƷFeCO3�ڿ����л�����������ˮ��������FeO��OH��������ʽΪ 4FeCO3+O2+2H2O=4FeO��OH��+4CO2���ʴ���
d����ҵ����NH4HCO3��FeSO4��Ӧ���Ʊ����ȸ��ߵ�FeCO3������ȷ��
�ʴ�Ϊ��ad��
���� ���⿼������ʵ�鷽����ƣ���Ŀ�Ѷ��еȣ����ؿ���ѧ���ķ������жϼ�ʵ�������������ȷʵ��ԭ�������������ǽⱾ��ؼ���Ҫ�����������ʵ�������ץס��Ŀ��Ϣ����ʵ��ʱ�ؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��������һ����Ҫ�����ȼ�ϣ�Ҳ�������������������ȣ��Գ��������ƻ����ã���ҵ�Ͽ�����ú���������ˮú�����ϳɶ����ѣ�
��������һ����Ҫ�����ȼ�ϣ�Ҳ�������������������ȣ��Գ��������ƻ����ã���ҵ�Ͽ�����ú���������ˮú�����ϳɶ����ѣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ��C��D��E������������Ӧˮ��������Եݼ� | |
| B�� | Ԫ��D��E�ֱ���Ԫ��A�γɻ�������ȶ��ԣ�A2D��AE | |
| C�� | D��E�����ӵĻ�ԭ��˳��Ϊ��D��E | |
| D�� | Ԫ��B��D��E�ļ����Ӱ뾶��СΪ��B��D��E |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��NH4+����c��Cl-����c��H+����c��OH-�� | B�� | c��NH4+����c��Cl-����c��OH-����c��H+�� | ||
| C�� | c��Cl-����c��NH4+����c��H+����c��OH-�� | D�� | c��Cl-����c��NH4+����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H6��C3H8 | B�� | C5H10��C6H6 | C�� | C2H6O��C2H4O2 | D�� | C3H6��C3H8O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4 | B�� | HCl | C�� | CH2=CH2 | D�� | F2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��A��=0.2mol•��L•s��-1�������������� | B�� | v��C��=0.5 mol•��L•s��-1 | ||
| C�� | v��B��=0.6 mol•��L•s��-1�������������� | D�� | v��D��=0.3 mol•��L•s��-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2��1 | B�� | 1��2 | C�� | 1��1 | D�� | 1��3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com