
 �����ô˸�������������ѧ���⣺
�����ô˸�������������ѧ���⣺ 4NO(g)��6H2O(g)�������¶ȱ��ֲ��䲢����He����ƽ��_______ ��������ƶ������������ƶ����������ƶ������� ����������� ______����д���������С�����䡱����
4NO(g)��6H2O(g)�������¶ȱ��ֲ��䲢����He����ƽ��_______ ��������ƶ������������ƶ����������ƶ������� ����������� ______����д���������С�����䡱���� C��g��+D��g���Ѵ�ƽ�����____________
C��g��+D��g���Ѵ�ƽ�����____________ 
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| �� |
| ||
| �� |
| 8a |
| 29 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��80��ʱ��0.40mol��N2O4������� 2L�Ѿ���յĹ̶��ݻ����ܱ������У���һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
| ������ʱ�䣨s�� n��mol�� | 0 | 20 | 40 | 60 | 80 | 100 |
| n��N2O4�� | 0.40 | a | 0.20 | c | d | e |
| n��NO2�� | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
��1������20s��40s����N2O4��ʾ��ƽ����Ӧ����Ϊ������������������������������
��2�������� 80��ʱ�÷�Ӧ��ƽ�ⳣ��K���� ������������������������������
��3�����жϸ÷�Ӧ�Ƿ��Ѵﻯѧƽ��״̬��������________________��
a��������ѹǿ����
b�����������c(N2O4)����
c��v��(NO2)��v��(N2O4)
d����������ܶȲ���
e����������ƽ��Ħ����������
f��c(N2O4)= c(NO2)
��4����Ӧ������100s��Ӧ�������¶Ƚ��ͣ�����������ɫ�������������������������������dz������������䡱����
��5��Ҫ����÷�Ӧ��Kֵ���ɲ�ȡ�Ĵ�ʩ�У�����ţ�����������������Ҫ���´ﵽƽ��ʱ��ʹ[NO2]/[N2O4]ֵ��С���ɲ�ȡ�Ĵ�ʩ�У�����ţ�������������������������������
A������N2O4����ʼŨ�ȡ�������B������������ͨ��NO2
C��ʹ�ø�Ч�������������� D�������¶�
��6������ͼ�� 80��ʱ������N2O4���ʵ����ı仯���ߣ����ڸ�ͼ�в������÷�Ӧ�� 60��ʱN2O4���ʵ����ı仯���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010���Ϻ��пؽ���ѧ��һ�ڶ�ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��֪�ڴ������������£��ܷ������·�Ӧ��
CO + H2O(g)  H2 + CO2 + Q
H2 + CO2 + Q
��1����5 Lʢ�й��������������ɺ��Բ��ƣ����ܱ������У�ͨ�뷴Ӧ�10 s������������0.2 g�����10 s��CO��ƽ����Ӧ����Ϊv(CO) = ____ _0.002 mol/Ls______��
��2���ڸ��ܱ������У�������������˵����Ӧ�Ѿ��ﵽƽ��״̬����__ BC___
A��������������䣬��һ���¶���ѹǿ�ﵽ�㶨
B��CO2������������H2O��������������֮��Ϊ1 : 1
C��CO��H2O��H2��CO�������е����ʵ���Ũ�ȱ��ֲ���
D����Ӧ��ϵ�л�����ƽ��Ħ���������ֲ���
��3����������Ӧ��ƽ��״̬�ֱ�ı��������������������ͼ��
A���ڵ�20 sʱ�����������С�� B���ڵ�20 sʱ����������ע��������
ԭ����һ���ѹǿ�仯ͼ CO��������淴Ӧ���ʱ仯ͼ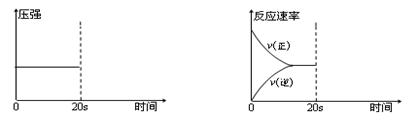
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��������·ʵ����ѧ������ѧ�ڵ������¿���ѧ�Ծ� ���ͣ������
��80��ʱ��0.40mol��N2O4������� 2L�Ѿ���յĹ̶��ݻ����ܱ������У���һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
|
������ʱ�䣨s�� n��mol�� |
0 |
20 |
40 |
60 |
80 |
100 |
|
n��N2O4�� |
0.40 |
a |
0.20 |
c |
d |
e |
|
n��NO2�� |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
��1������20s��40s����N2O4��ʾ��ƽ����Ӧ����Ϊ���� ��������������������������
��2�������� 80��ʱ�÷�Ӧ��ƽ�ⳣ��K���� ������������������������������
��3�����жϸ÷�Ӧ�Ƿ��Ѵﻯѧƽ��״̬��������________________��
a��������ѹǿ����
b�����������c(N2O4)����
c��v��(NO2)��v��(N2O4)
d����������ܶȲ���
e����������ƽ��Ħ����������
f��c(N2O4)= c(NO2)
��4����Ӧ������100s��Ӧ�������¶Ƚ��ͣ�����������ɫ�� �����������������������������dz������������䡱����
��5��Ҫ����÷�Ӧ��Kֵ���ɲ�ȡ�Ĵ�ʩ�У�����ţ�����������������Ҫ���´ﵽƽ��ʱ��ʹ[NO2]/[N2O4]ֵ��С���ɲ�ȡ�Ĵ�ʩ�У�����ţ�������������������������������
A������N2O4����ʼŨ�ȡ�������B������������ͨ��NO2
C��ʹ�ø�Ч�������������� D�������¶�
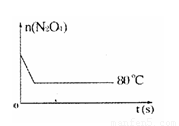
��6������ͼ�� 80��ʱ������N2O4���ʵ����ı仯���ߣ����ڸ�ͼ�в������÷�Ӧ�� 60��ʱN2O4���ʵ����ı仯���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010���Ϻ��и�һ�ڶ�ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��֪�ڴ������������£��ܷ������·�Ӧ��
CO + H2O(g)  H2 + CO2 + Q
H2 + CO2 + Q
��1����5 Lʢ�й��������������ɺ��Բ��ƣ����ܱ������У�ͨ�뷴Ӧ�10 s������������0.2 g�����10 s��CO��ƽ����Ӧ����Ϊv(CO) = ____ _______��
��2���ڸ��ܱ������У�������������˵����Ӧ�Ѿ��ﵽƽ��״̬����__ ___
A��������������䣬��һ���¶���ѹǿ�ﵽ�㶨
B��CO2������������H2O��������������֮��Ϊ1 : 1
C��CO��H2O��H2��CO�������е����ʵ���Ũ�ȱ��ֲ���
D����Ӧ��ϵ�л�����ƽ��Ħ���������ֲ���
��3����������Ӧ��ƽ��״̬�ֱ�ı��������������������ͼ��
A���ڵ�20 sʱ�����������С�� B���ڵ�20 sʱ����������ע��������
ԭ����һ���ѹǿ�仯ͼ CO��������淴Ӧ���ʱ仯ͼ

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com