
科目:高中化学 来源:2015-2016学年江西省高一下学期第四次月考化学试卷(解析版) 题型:选择题
为体现“绿色奥运”“科技奥运”,2008年北京奥运会出现中国自己生产的燃料电池汽车,作为马拉松领跑车和电视拍摄车,预计该车装着“绿色心脏”——质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是( )
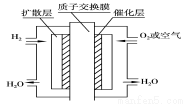
A.通入氧气的电极发生氧化反应
B.通入氢气的电极为正极
C.总反应式为O2+2H2点燃2H2O
D.正极的电极反应式为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下期末化学试卷(解析版) 题型:选择题
下列变化属于物理变化的是
A.煤的干馏 B.石油的分馏 C.铁器生锈 D.红磷转化为白磷
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下学期期中化学试卷(解析版) 题型:选择题
下列各组粒子中属于同位素的是( )
A. 16O和18O B. H2O和D2O C. H2和D2 D. 24Mg和24Na
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高二下学期期中化学试卷(解析版) 题型:选择题
分子式为C9H18O2的有机物A,在硫酸存在下与水反应生成B、C两种物质,C经一系列氧化最终可转化为B的同类物质,又知等质量的B、C的蒸气在同温同压下所占体积相同,则A的酯类同分异构体共有(包括A) ( )
A.8种 B.12种 C.16种 D.18种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆农业大学附中高二下学期期中化学试卷(解析版) 题型:填空题
合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
据此回答以下问题:
(1)①该反应的化学平衡常数表达式为K=________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越________。
(2)某温度下,若把1 mol N2与3 mol H2置于体积为1L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为1/3,则该温度下反应的K的计算式=________(用分数表示)。能说明该反应达到化学平衡状态的是________(填字母)。
a.容器内的密度保持不变
b.容器内压强保持不变
c.v正(N2)=2v逆(NH3)
d.混合气体中c(NH3)不变
(3)对于合成氨反应而言,下列有关图像一定正确的是(选填序号)________。
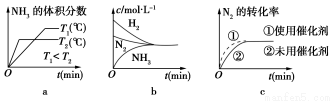
(4)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a________b(填“>”、“=”或“<”,下同),Q1________Q2,Q1________92.4。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com