
| A. | 向Na2CO3溶液中加入甲酸无明显现象产生 | |
| B. | 25℃时,向甲酸中加入NaOH溶液,HCOOH的电离程度和K均增大 | |
| C. | 向碳酸中加入NaHCO3固体,c(H+)减小 | |
| D. | 向0.1 mol•L-1甲酸中加入蒸馏水,c(H+)增大 |
分析 A.电离常数越大,酸性越强,酸性强的可以制酸性弱的;
B.电离常数只与温度有关;
C.NaHCO3电离出的碳酸氢根离子抑制碳酸的电离;
D.甲酸的稀溶液中加水稀释,氢离子浓度减小.
解答 解:A.电离常数越大,酸性越强,酸性强的可以制酸性弱的,甲酸的酸性大于碳酸,所以向Na2CO3溶液中加入甲酸会生成二氧化碳气体,故A错误;
B.电离常数只与温度有关,25℃时,向甲酸中加入NaOH溶液,氢离子浓度减小,HCOOH的电离程度增大,K不变,故B错误;
C.NaHCO3电离出的碳酸氢根离子抑制碳酸的电离,溶液中氢离子浓度减小,故C正确;
D.甲酸的稀溶液中加水稀释,促进甲酸的电离,氢离子的物质的量增大,溶液的体积也增大,由于体积增大的快,所以氢离子浓度减小,故D错误.
故选C.
点评 本题考查了弱电解质的电离,明确酸性强弱与其电离程度、电离常数的关系是解本题关键,难度中等,侧重于考查学生的分析能力.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:实验题
人们获得食盐的方式有多种,最主要的是海水晒盐。通过海水晾晒得到的粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是制备精盐的实验流程(试剂以化学式表示)

(1)BaCl2、NaOH、Na2CO3的加入顺序,必须保证___________在____________后
(2)溶解、过滤、蒸发过程中都使用到的玻璃仪器是_______ _________,蒸发时玻璃棒的作用是______________________
(3)经过⑤步骤之后得到的沉淀的成分为:________________________
(4)制得的精盐中不小心混入了硝酸钾晶体,用电子天平称取8.00g样品溶于水,向溶液中加入足量硝酸银溶液,将产生的沉淀过滤、洗涤、干燥,并称得其质量为14.35g,则该样品中氯化钠的质量分数为______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:选择题
将5mol/L盐酸10mL稀释到200mL,再取出5mL,这5mL溶液的物质的量浓度为
A.0.05mol/L B.0.25mol/L C.0.1mol/L D.0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | V1≤V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
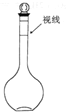 欲配制100ml 1.0mol/L Na2SO4溶液,下列说法正确的是( )
欲配制100ml 1.0mol/L Na2SO4溶液,下列说法正确的是( )| A. | ②④ | B. | ②③ | C. | ①③ | D. | 以上都不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸碱中和滴定终点的pH值一定等于7 | |
| B. | 滴定实验中锥形瓶不可用待测液润洗 | |
| C. | 滴定实验中,KMnO4溶液应放在碱式滴定管中 | |
| D. | 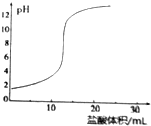 用盐酸滴定NaOH溶液的滴定曲线如图所示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为566kJ•mol-1 | |
| B. | 2 mol CO和1 mol O2的总能量比2 mol CO2的总能量低 | |
| C. | 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1453.28 kJ•mol-1 | |
| D. | 完全燃烧16g甲醇,生成一氧化碳和水时放出的热量为221.82 kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com