
【题目】根据下列化合物:①NaCl ②NaOH ③HCl ④NH4Cl ⑤CH3COONa ⑥CH3COOH ⑦NH3H2O ⑧H2O,回答下列问题.
(1)NH4Cl溶液显酸性,用离子方程式表示原因 ,其溶液中离子浓度大小顺序为 。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH﹣)= ,在pH=3的CH3COOH溶液中,水电离出来的c(H+)= 。
(3)若将等pH、等体积的②NaOH和⑦NH3H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m n。(填“<”、“>”或“=”)
(4)若前五种溶液的物质的量浓度相同,用序号排出这五种溶液pH由大到小的顺序 。
【答案】(1)NH4++H2O![]() NH3H2O+H+ c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)
NH3H2O+H+ c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣)
(2)c(OH﹣)=10-3molL﹣1 ;c(H+)=10-11molL﹣1 (3)m<n (4)②>⑤>①>④>③
【解析】
试题分析:(1)NH4Cl是强酸弱碱盐,铵根水解溶液显酸性,水解方程式为NH4++H2O![]() NH3H2O+H+。由于铵根的水解程度很小,所以溶液中离子浓度大小顺序为c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣);
NH3H2O+H+。由于铵根的水解程度很小,所以溶液中离子浓度大小顺序为c(Cl﹣)>c(NH4+)>c(H+)>c(OH﹣);
(2)常温下,pH=11的CH3COONa溶液中,醋酸根水解,溶液显碱性,则水电离出来的c(OH﹣)=10-3molL﹣1 ;在pH=3的CH3COOH溶液中,醋酸电离抑制水的电离,则水电离出来的c(H+)=10-11molL﹣1。
(3)由于氢氧化钠是强碱,稀释过程中氢氧根的物质的量不变,一水合氨是弱电解质,稀释促进电离,所以若将等pH、等体积的②NaOH和⑦NH3H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m<n。
(4)NaCl是强酸强碱盐,溶液显中性;NaOH是一元强碱;HCl是一元强酸;NH4Cl是强酸弱碱盐,铵根水解,溶液显酸性;CH3COONa是强碱弱酸盐,醋酸根水解,溶液显碱性,所以若五种溶液的物质的量浓度相同,则这五种溶液pH由大到小的顺序②>⑤>①>④>③,


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】250℃和 1.01×105Pa时,2N2O5(g)= 4NO2(g)+ O2(g) △H=+56.76 kJ/mol 能自发进行,其自发进行的原因是
A.是吸热反应
B.是放热反应
C.是熵减少的反应
D.熵增效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.Fe(NO3)2溶液中滴入一定量盐酸:3Fe2++4H++NO3-=2H2O+NO↑+3Fe3+
B.向氯化铵的溶液中加入足量浓NaOH溶液并加热:NH4++OH-![]() NH3·H2O
NH3·H2O
C.Ba(OH)2溶液与H2SO4溶液混合产生沉淀:Ba2++ SO42-=BaSO4↓
D.往NaOH溶液中通入过量SO2:SO2+2OH-=SO32- +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铁生锈的过程为:Fe → Fe(OH)2 → Fe(OH)3 → Fe2O3·xH2O。又知草酸(H2C2O4)分解产生CO等气体某化学小组为测定两种不同生锈铁片的组成(设只含有铁和Fe2O3·xH2O),进行了以下探究,请你参与并完成对有关问题的解答。
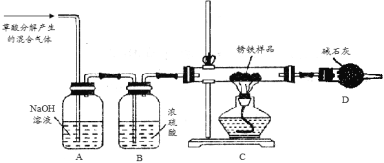
(1)甲同学利用草酸分解产生的混合气体和下图所示装置测定其中一种锈铁的组成。
主要操作为:取锈铁样品12.6 g置于装置C的硬质玻璃管中,加热完全反应后得到固体的质量为8.4 g,装置D增重8.4 g。
草酸(H2C2O4)分解的化学方程式为 。
(2)乙同学在甲同学装置的基础上将装置D换成装浓硫酸的洗气瓶(装置E,此装置图略),经改进后,重新按甲同学的操作和样品取用量进行实验,若完全反应后得到固体的质量仍为8.4 g,而装置E增重1.8 g,则x = ;m(Fe):m (Fe2O3·xH2O) =
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的工具和基础。下列有关化学用语的使用正确的是( )
A.用食醋除去水壶内的水垢:CaCO3+2H+=Ca2++CO2↑+H2O
B.纯碱溶液呈碱性的原因是:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C.钢铁发生吸氧腐蚀的正极反应式:O2+4e-+2H2O=4OH-
D.表示氢气燃烧热的热化学方程式为2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ· mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备
过氧化钙的实验方法。回答下列问题:
(一)碳酸钙的制备

步骤①加入氨水的目的是________________。小火煮沸的作用是使沉淀颗粒长大,有利于__________________。
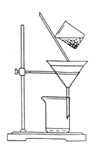
(2)如图是某学生的过滤操作示意图,其操作不规范的是_________(填标号)。
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备
![]()
(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈_______性(填“酸”、“碱”或“中”)。将溶液煮沸,趁热过滤。将溶液煮沸的作用是______________。
(4)步骤③中反应的化学方程式为____________________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是___________。
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是______________,产品的缺点是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com