
| A. | -1 528.6 kJ•mol-1 | B. | -1 473 kJ•mol-1 | ||
| C. | +1 473 kJ•mol-1 | D. | +1 528.6 kJ•mol-1 |
分析 由信息可知,①SO42-(aq)+Ba2+(aq)+2OH-(aq)+2H+(aq)=BaSO4(s)↓+2H2O(l)△H=-1 584.2kJ•mol-1;
②OH-(aq)+H+(aq)=H2O(l)△H=-55.6kJ•mol-1,
由盖斯定律可知,①-②×2得到SO42-(aq)+Ba2+(aq)=BaSO4(s),以此来解答.
解答 解:由信息可知,①SO42-(aq)+Ba2+(aq)+2OH-(aq)+2H+(aq)=BaSO4(s)↓+2H2O(l)△H=-1 584.2kJ•mol-1;
②OH-(aq)+H+(aq)=H2O(l)△H=-55.6kJ•mol-1,
由盖斯定律可知,①-②×2得到SO42-(aq)+Ba2+(aq)=BaSO4(s),其反应热为(-1 584.2kJ•mol-1)-(-55.6kJ•mol-1)×2=-1 473 kJ•mol-1,
故选B.
点评 本题考查反应热与焓变,为高频考点,把握已知反应与目标反应的关系为解答的关键,侧重分析与计算能力的考查,注意盖斯定律的应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 44g二氧化碳气体中含有共用电子对数目为2NA | |
| B. | 室温下,1L0.1 mol•L-1的Na2CO3溶液中,CO32-离子数目为0.1NA | |
| C. | 6.0g碳在8.4L氧气(标准状况)中燃烧,转移的电子数为1.5NA | |
| D. | 500mL1.0mol•L-1盐酸与0.435gMnO2共热后,生成Cl2分子的数目为0.005NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外有13个电子,核内有13个质子 | |
| B. | 质量数为13,原子序数为6,核内有7个质子 | |
| C. | 136C与126C互为同位素 | |
| D. | 质量数为13,质子数为6,中子数为6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
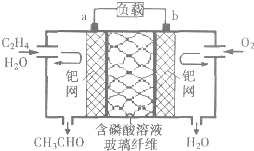
| A. | a电极为正电极 | |
| B. | 放电时,若有2mol电子转移,则理论上需要消耗28g乙烯 | |
| C. | a极的电极反应式为CH2═CH2+2OH--2e-═CH3CHO+H2O | |
| D. | 电子移动方向:a电极→磷酸溶液→b电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的氧化性比I2的强 |
| D | 取少量食盐溶于水,加稀硫酸酸化,再滴入淀粉溶液,溶液未呈蓝色 | 该食盐中不含有碘酸钾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LSO3所含的氧原子数为1.5NA | |
| B. | 常温常压下,7.8gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8NA | |
| C. | 电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA | |
| D. | 500ml 1mol/L醋酸溶液中含氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
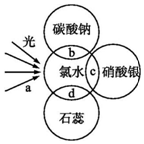 氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)
氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的分子数目之比是 4:5 | B. | 它们的氧元素的质量之比为 2:3 | ||
| C. | 它们的物质的量之比为 5:4 | D. | 它们的密度之比为 5:4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com