
| A. | 用NaOH溶液来鉴别NH4Cl和KCl | |
| B. | 用硝酸酸化的AgNO3溶液来鉴别NH4Cl和NH4NO3 | |
| C. | 某溶液中滴加BaCl2溶液后产生白色沉淀,则该溶液中一定含有SO42-离子 | |
| D. | 用焰色反应鉴别NaCl和KNO3 |
分析 A.氯化铵与碱反应生成刺激性气体,而KCl不能;
B.NH4Cl与硝酸银反应生成白色沉淀,而硝酸铵不能;
C.白色沉淀可能为AgCl;
D.Na、K的焰色反应分别为黄色、紫色.
解答 解:A.氯化铵与碱反应生成刺激性气体,而KCl不能,则用NaOH溶液可鉴别NH4Cl和KCl,故A正确;
B.NH4Cl与硝酸银反应生成白色沉淀,而硝酸铵不能,则用硝酸酸化的AgNO3溶液可鉴别NH4Cl和NH4NO3,故B正确;
C.白色沉淀可能为AgCl,则某溶液中滴加BaCl2溶液后产生白色沉淀,则该溶液中不一定含有SO42-离子,故C错误;
D.Na、K的焰色反应分别为黄色、紫色,则焰色反应可鉴别,故D正确;
故选C
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的鉴别、离子的检验等,把握物质的性质、元素化合物知识为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
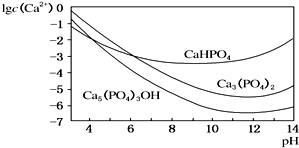 羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料,其常用的制备方法有两种:
羟基磷灰石[Ca5(PO4)3OH]是一种重要的生物无机材料,其常用的制备方法有两种:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒).持续通入甲烷,在标准状况下,消耗甲烷的体积为V L.
将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒).持续通入甲烷,在标准状况下,消耗甲烷的体积为V L.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L | B. | 2L | C. | 3L | D. | 2.8 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的化学式:HClO2 | B. | 硫离子的结构示意图: | ||
| C. | 质量数为127的钡原子:127Ba | D. | 氨气(NH3)中氮元素的化合价:+3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 火药使用 | 粮食酿酒 | 转轮排字 | 铁的冶炼 |
 |  |  |  |
| 用品 |  |  |  |  |
| 有效成分 | NaCl | NaOH | NaHCO3 | Ca(ClO)2 |
| 用途 | 做调味品 | 做治疗胃病的抗酸药 | 做发酵粉 | 做消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 相同温度下,Na2CO3的溶解度大于NaHCO3 | |
| B. | NaHCO3比Na2CO3热稳定性强 | |
| C. | Na2CO3和NaHCO3均可与澄清石灰水反应 | |
| D. | Na2CO3和NaHCO3均不与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com