
某可逆反应过程能量变化如图所示,下列说法中正确的是( )

A.该反应热化学方程式为A(g)+2B(g)  3C(g)+D(g) ΔH>0
3C(g)+D(g) ΔH>0
B.其他条件不变,升高温度,A的转化率增大
C.其他条件不变,增大压强,释放热量减少,平衡常数K减小
D.其他条件不变,加催化剂,反应速率增大,E1和E2均减小,ΔH不变
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2015届北京市怀柔区高二上学期期末质量检测化学试卷(解析版) 题型:选择题
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列事实不能说明上述观点的是
A.乙烯能发生加成反应,乙烷不能发生加成反应
 B.苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应
B.苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应
C.甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色
D.苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题8溶液中的离子反应练习卷(解析版) 题型:选择题
下图是向100 mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图像,根据如图所得结论正确的是( )
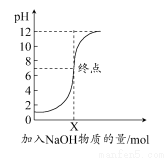
A.原来盐酸的物质的量浓度为0.1 mol·L-1
B.NaOH溶液的浓度为0.1 mol·L-1
C.原来盐酸的物质的量浓度为1 mol·L-1
D.NaOH溶液的浓度为0.01 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:H2NCOONH4(s)  2NH3(g)+CO2(g),在不同温度下,该反应平衡状态时的部分数据见下表。下列说法正确的是( )
2NH3(g)+CO2(g),在不同温度下,该反应平衡状态时的部分数据见下表。下列说法正确的是( )
温度 | 平衡浓度/(mol·L-1) | |
c(NH3) | c(CO2) | |
T1 | 0.1 |
|
T2 |
| 0.1 |
A.若T2>T1,则该反应的ΔH<0
B.向容器中充入N2,H2NCOONH4质量增加
C.NH3体积分数不变时,说明该反应达到平衡
D.T1、T2时,H2NCOONH4转化的Δn(T2)=2Δn(T1)
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)  2HI(g) ΔH<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )
2HI(g) ΔH<0,当达到平衡后,t0时若保持混合气体总物质的量不变而改变某一反应条件,使容器内压强增大(如图所示),下列说法正确的是( )

A.容器内气体颜色变深,平均相对分子质量不变
B.平衡不移动,混合气体密度不变
C.H2转化率增大,HI平衡浓度减小
D.t0时改变的条件是减小体积或升高体系温度
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题6化学反应与能量变化练习卷(解析版) 题型:填空题
用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2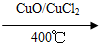 2Cl2+2H2O
2Cl2+2H2O
(1)已知:ⅰ.反应A中,4 molHCl被氧化,放出115.6 kJ的热量。
ⅱ.
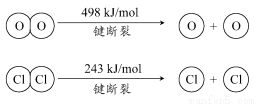
①H2O的电子式是________。
②反应A的热化学方程式是______________________________________。
③断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为________kJ,H2O中H—O键比HCl中H—Cl键(填“强”或“弱”)________。
(2)对于反应A,下图是在4种投料比[n(HCl):n(O2),分别为1:1、2:1、4:1、6:1]下,反应温度对HCl平衡转化率影响的曲线。
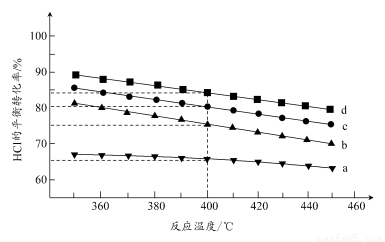
①曲线b对应的投料比是________。
②当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度与投料比的关系是______________________________。
③投料比为2:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题6化学反应与能量变化练习卷(解析版) 题型:选择题
某些化学键键能数据如下:
化学键 | H—H | Cl—Cl | H—Cl |
键能/ kJ·mol-1 | 436 | 243 | 431 |
则下列热化学方程式不正确的是( )
A. 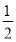 H2(g)+
H2(g)+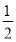 Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1
Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g)ΔH=-183 kJ·mol-1
C. 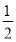 H2(g)+
H2(g)+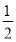 Cl2(g)=HCl(g)ΔH=+91.5 kJ·mol-1
Cl2(g)=HCl(g)ΔH=+91.5 kJ·mol-1
D.2HCl(g)=H2(g)+Cl2(g)ΔH=+183 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题5微观结构与物质的多样性练习卷(解析版) 题型:选择题
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
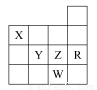
A.常压下五种元素的单质中W单质的沸点最高
B.Z元素的最高价氧化物对应的水化物酸性最强
C.X的氢化物比同族元素的氢化物沸点低
D.Y、Z和W的阴离子半径依次增大
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题2从海水中获得的化学物质练习卷(解析版) 题型:选择题
把一块镁铝合金投入到1 mol/L盐酸里,待合金完全溶解后,往溶液里加入1 mol/L NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图A所示。下列说法中不正确的是( )
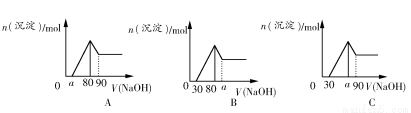
A.a的取值范围为0≤a<50
B.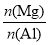 的最大值为2.5
的最大值为2.5
C.若将关系图改为图B,则a的取值范围为80<a<90
D.若将关系图改为图C,则a的取值范围为75<a<90
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com