
| 1 |
| 2 |
| 时间/S | 0 | 500 |
| c(SO2)mol?L-l | 5.00 | 3.52 |
| 10 |
| 3 |
| 5-3.52 |
| 500 |
| v(SO2) |
| 2 |
| ||||||
|
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1.5 |
| 2 |


科目:高中化学 来源: 题型:
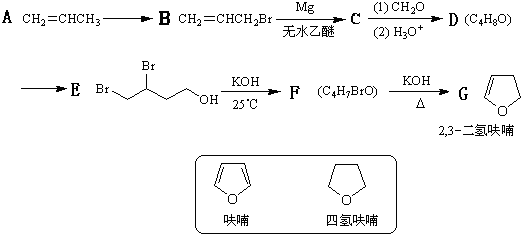

查看答案和解析>>
科目:高中化学 来源: 题型:
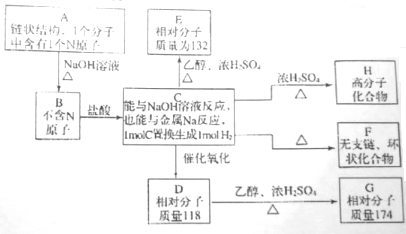
查看答案和解析>>
科目:高中化学 来源: 题型:
 利用有关知识回答下列问题:
利用有关知识回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
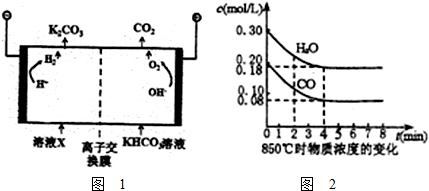
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应温度必须控制在170℃ |
| B、反应物是乙醇和过量的3mol/L硫酸的混合液 |
| C、温度计应插入反应溶液液面以下 |
| D、反应容器中应加入少许瓷片 |
查看答案和解析>>
科目:高中化学 来源: 题型:
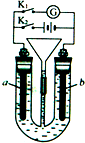 在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.
在如图所示装置中,U形管内装满稀H2SO4,a为铁电极,b为多孔石墨电极.查看答案和解析>>
科目:高中化学 来源: 题型:
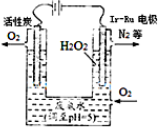 最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图
最近华南理工大提出利用电解法制H2O2并用产生的H2O2处理废氨水,装置如图查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验②证明Fe2+既有氧化性又有还原性 |
| B、实验③生成的气体不能使湿润的淀粉KI试纸变蓝 |
| C、上述实验中,有三个氧化还原反应 |
| D、上述实验证明氧化性:MnO2>MnO4->Cl2>Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com