

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������£����ʵ���Ũ�Ⱦ�Ϊ0.1mol��L?1Na2CO3��NaHCO3�ĵ���������Һ�У� 2c(OH?)��2c(H+)��3c(H2CO3)��c(HCO3��)��c(CO32?) |
| B����H��0,��S��0�ķ�Ӧ�����Է���Ӧ����H��0,��S��0�ķ�Ӧ�κ��������Ƿ��Է���Ӧ�� |
| C����֪��P4(g)��6Cl2(g)��4PCl3(g) ��H��akJ��mol��1 P4(g)��10Cl2(g)��4PCl5(g)��H��bkJ��mol��1 P4������������ṹ��PCl5��P��Cl���ļ���ΪckJ��mol��1,PCl3��P��Cl���ļ���Ϊ1.2ckJ��mol��1���ɴ˼���Cl��Cl���ļ��� 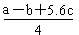 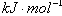 |
D����һ���¶��£��̶����Ϊ2L�ܱ������У�������Ӧ��2SO2(g)+O2(g) 2SO3(g) 2SO3(g) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 H2O(l)����H="-57.3" kJ��mol-1,��֪����ʵĵ��������ȹ��̡���1 L 0.5 mol��L-1��NaOH��Һ�м�����������:��ϡ����;��Ũ����;��ϡ����,ǡ����ȫ��Ӧ�����ʱ䦤H1����H2����H3�Ĺ�ϵ��(����)
H2O(l)����H="-57.3" kJ��mol-1,��֪����ʵĵ��������ȹ��̡���1 L 0.5 mol��L-1��NaOH��Һ�м�����������:��ϡ����;��Ũ����;��ϡ����,ǡ����ȫ��Ӧ�����ʱ䦤H1����H2����H3�Ĺ�ϵ��(����)| A����H1>��H2>��H3 | B����H1<��H3<��H2 |
| C����H1=��H3>��H2 | D����H1>��H3>��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
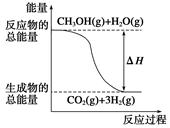
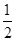 O2(g)=CO2(g)��2H2(g) ��H����192.9 kJ��mol��1
O2(g)=CO2(g)��2H2(g) ��H����192.9 kJ��mol��1| A��CH3OH��ȼ����Ϊ192.9 kJ��mol��1 |
| B����Ӧ���е������仯��ͼ��ʾ |
| C��CH3OHת���H2�Ĺ���һ��Ҫ�������� |
D�����ݢ���֪��Ӧ��CH3OH(l)��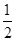 O2(g)=CO2(g)��2H2(g)�Ħ�H����192.9 kJ��mol��1 O2(g)=CO2(g)��2H2(g)�Ħ�H����192.9 kJ��mol��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ʯ�� | B������NaCl | C����ˮ�Ҵ� | D������NH4NO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

 NH4++ NH2����ij�¶�ʱ�������ӻ�K=2��l0-30�����¶��£��ٽ�����NH4Cl�������Һ���У�K____________2��10-30�����������������=�������ڽ�����������Ͷ��Һ���У���ȫ��Ӧ��������Һ�и�����Ũ�ȴ�С��ϵΪ��_______
NH4++ NH2����ij�¶�ʱ�������ӻ�K=2��l0-30�����¶��£��ٽ�����NH4Cl�������Һ���У�K____________2��10-30�����������������=�������ڽ�����������Ͷ��Һ���У���ȫ��Ӧ��������Һ�и�����Ũ�ȴ�С��ϵΪ��_______| A��c(NH4+)/c(NH3?H2O) | B��c(NH3?H2O)/c(OH-) |
| C��c(H+)/c(NH4+) | D��c(OH-)/c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
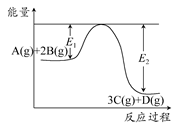
A���÷�Ӧ�Ȼ�ѧ����ʽΪA(g)��2B(g)  3C(g)��D(g)����H>0 3C(g)��D(g)����H>0 |
| B�������������䣬�����¶ȣ�A��ת�������� |
| C�������������䣬����ѹǿ���ͷ��������٣�ƽ�ⳣ��K��С |
| D�������������䣬�Ӵ�������Ӧ��������E1��E2����С����H���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3��g���������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ1��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
2SO3��g���������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ1��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
 2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����ƽ�� �ƶ�������������ҡ���������
2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����ƽ�� �ƶ�������������ҡ����������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com