
A、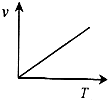 |
B、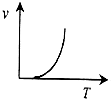 |
C、 |
D、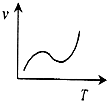 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.24 mol |
| B、0.21 mol |
| C、0.25 mol |
| D、0.14 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
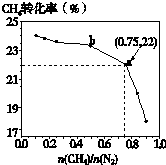 已知:3CH4(g)+2N2(g)
已知:3CH4(g)+2N2(g)| 700℃ |
| 催化剂 |
| n(CH4) |
| n(N2) |
A、
| ||
B、
| ||
| C、b点对应的平衡常数比a点的大 | ||
| D、a点对应的NH3的体积分数约为26% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可能是Al3+,也可能是Mg2+ |
| B、只能是Al3+ |
| C、只能是Mg2+ |
| D、以上说法都不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
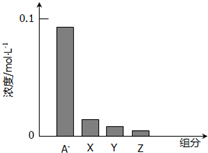 常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )| A、HA为强酸 |
| B、该混合液pH=7 |
| C、图中X表示HA,Y表示OH-,Z表示H+ |
| D、该混合溶液中:c(A-)+c(Y)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
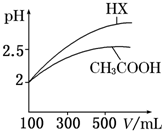 回答下列问题:
回答下列问题:| c(H+) |
| c(CH3COOH) |
| c(OH-) |
| c(H+) |
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com