
| A. | .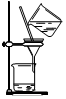 装置可用于除去乙醇中的溴苯 | |
| B. | .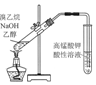 用图所示装置检验溴乙烷与NaOH醇溶液共热产生的C2H4 | |
| C. | .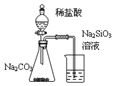 装置可证明非金属性Cl>C>Si | |
| D. | 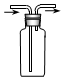 装置可用于收集O2 |
分析 A.溴苯易溶于乙醇,无法通过过滤操作分离;
B.乙醇易挥发,挥发出的乙醇能够使酸性高锰酸钾溶液褪色;
C.稀盐酸易挥发,干扰了C、Si非金属性强弱判断,且稀盐酸不是含氧酸;
D.氧气的密度大于空气,且不与空气中各组分反应.
解答 解:A.乙醇为有机溶剂,混合液没有沉淀,无法利用过滤操作除去乙醇中的溴苯,应该用蒸馏操作完成,故A错误;
B.乙烯中混有乙醇,乙醇也能够使酸性高锰酸钾溶液褪色,干扰了检验结果,故B错误;
C.稀盐酸不是含氧酸,且挥发出的盐酸能够使硅酸钠变浑浊,图示装置无法达到实验目的,故C错误;
D.氧气的密度大于空气,可以用向上排空气法收集,图示操作合理,能够达到实验目的,故D正确;
故选D.
点评 本题考查化学实验方案的评价,题目难度不大,涉及物质分离与提纯、气体收集、非金属性强弱比较等知识,明确常见化学实验基本操作方法即可解答,试题有利于提高学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | ②③④⑥ | B. | ③④⑥⑦ | C. | ③④⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 此反应不属于化学变化 | |
| B. | 112 号元素的相对原子质量为 227 | |
| C. | 科学家合成的 112 号元素的原子的中子数为 165 | |
| D. | 112 号元素属于第七周期元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,2,3,3 四甲基丁烷 | B. | 2,3,4 三甲基戊烷 | ||
| C. | 3,3,4,4 四甲基己烷 | D. | 2,5 二甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

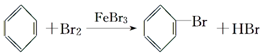
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢铵溶液与足量氢氧化钠溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | 将少量氯化铁溶液滴入硫化钠溶液中:2Fe3++S2-═2Fe2++S↓ | |
| C. | 向Fe(NO3) 2稀溶液中加入盐酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| D. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
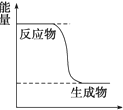 CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料.
CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
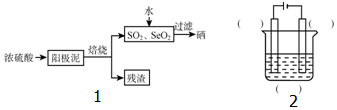
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com