
| A、Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
| B、用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O |
| C、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| D、氨水与醋酸反应:NH3?H2O+CH3COOH?CH3COO-+NH4++H2O |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
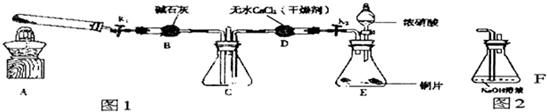
 用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( )
用图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( )| A、上下移动①中铜丝可控制反应开始停止 |
| B、若②中是澄清石灰水,先浑浊后澄清 |
| C、③中KMnO4溶液褪色,说明SO2有还原性 |
| D、①中铜丝换成光亮的铁丝,则因铁丝钝化而无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某原子的质量数为A,则该原子的相对原子质量也为A |
| B、稀有气体元素原子的最外层电子数均为8 |
| C、第二周期第ⅣA族元素的原子核电荷数和中子数一定为6 |
| D、原子序数为16的元素位于元素周期表的第三周期第ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 | 现象 | 结论 |
| A |  左边烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 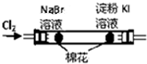 左边棉花变橙色,右边棉花变蓝色 | 氧化性:Cl2>Br2>I2 |
| C |  白色固体先变为浅黄色,后变为黑色 | 溶解性:AgCl<AgBr<Ag2S |
| D | 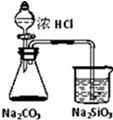 锥形瓶中有气体产生,烧杯中溶液变浑浊 | 酸性:盐酸>碳酸>硅酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4 |
| B、C2H5 |
| C、C2H6 |
| D、C4H10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4、C2H6、C3H8 |
| B、C2H4、C2H6、CH4 |
| C、CH4、C2H2、C2H6 |
| D、C2H6、C3H6、C4H6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com