
丙酸的结构为CH3—CH2—COOH,丙酸盐是安全有效的防霉、防腐剂,一种以碱式碳酸锌为原料的生产工艺流程如下: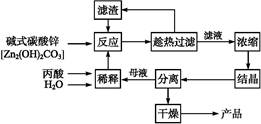
| 序号 | n(丙酸)∶ n(碱式碳酸锌) | 反应温度/℃ | 丙酸锌产率/% |
| 1 | 1∶0.25 | 60 | 67.2 |
| 2 | 1∶0.25 | 80 | 83.5 |
| 3 | 1∶0.25 | 100 | 81.4 |
| 4 | 1∶0.31 | 60 | 89.2 |
| 5 | 1∶0.31 | 80 | 90.1 |
| 6 | 1∶0.31 | 100 | 88.8 |
 ,反应温度 ℃。
,反应温度 ℃。  挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:填空题
【选修2:化学与技术】(15分)
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
(1)步骤④的离子反应方程式为 。
(2)溴微溶于水,步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,它们的相对密度相差较大。分离出液溴的实验室方法为 。
(3)步骤⑥如果在实验室中进行,需用到的玻璃仪器有 。
(4)工业生产不直接蒸馏含溴的海水得到液溴,而要经过“空气吹出、SO2吸收、氯化”,原因是 。
(5)苦卤水还可以用于制取金属镁,用化学方程式表示从苦卤水制取金属镁的反应原理 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是某工厂对海水资源进行综合利用的示意图。
请回答下列问题:
(1)请列举一种海水淡化的方法 。
(2)工业上常用离子交换膜电解槽生产NaOH,电解过程中大量通过离子交换膜的离子是 ,NaOH在电解槽的 室生成,由饱和食盐水制取NaOH的化学方程式为 。
(3)侯氏制碱法中向饱和食盐水中通入CO2和NH3制得NaHCO3,先通入 (填化学式),理由是 。再由NaHCO3制得纯碱,化学方程式为 。
(4)镁是一种用途很广泛的金属材料,目前世界上60%的镁从海水中提取。已知有关物质的熔沸点数据如下:
| | MgO | MgCl2 |
| 熔点/℃ | 2 852 | 714 |
| 沸点/℃ | 3 600 | 1 412 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为____________________;加入硅、锰和铝的目的是________________________。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹________(填“前”或“后”)加入,原因是______________________。
(4)炼铁和炼钢生产中,尾气中均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧—钠氧化法”回收Na2Cr2O7等物质。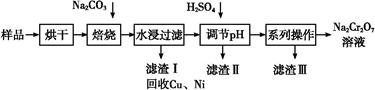
已知:在Na2CrO4溶液中含有少量NaAlO2、Na2ZnO2等物质
(1)水浸后的溶液呈 性(填“酸”、“碱”或“中”)。
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式。
Cr(OH)3+ Na2CO3+  Na2CrO4+ CO2+
Na2CrO4+ CO2+
(3)滤渣Ⅱ的主要成分有Zn(OH)2、 。
(4)“系列操作”中为:继续加入H2SO4, ,冷却结晶,过滤。继续加入H2SO4目的是 。
已知:①除去滤渣II后,溶液中存在如下反应:
2CrO42—+2H+ Cr2O72—+H2O
Cr2O72—+H2O
②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
| 温度 溶解度 化学式 | 20 ℃ | 60 ℃ | 100 ℃ |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在元素周期表中,铝在硼的正下方,它们有很多相似的化学性质,可以形成许多组成和性质类似的化合物。单质硼可以通过硼镁矿Mg2B2O5·H2O来制取。
(1)写出步骤①的化学方程式 ,
(2)写出步骤②的离子方程式 ,
(3)写出表示溶液a物料守恒的关系 ;
(4)步骤③中加入稀H2SO4的作用是 ;
(5)将制得的粗硼在一定条件下反应全部生成BI3,BI3热分解可以得到纯净的单质硼。0.25 g粗硼制成的BI3分解得到的I2全部被收集后,用2.00 mol/L Na2S2O3溶液滴定,达到滴定终点时消耗27.00 mL Na2S2O3溶液。(已知:I2+2S2O32- 2I-+S4O62-)
2I-+S4O62-)
①滴定过程中所用的指示剂为 ,滴定终点的现象是 ;
②粗硼中硼的含量为____ ;
(6)利用硼砂晶体(Na2B4O7?10H2O)可制备过硼酸钠,它是一种优良的漂白剂,被广泛应用于洗衣粉、漂白粉、洗涤剂中。已知纯净的过硼酸钠晶体中各元素的物质的量之比为以n(Na):n(B):n(H):n(O)=1:1:n:7。取过硼酸钠晶体在70℃以上加热将逐步失去结晶水,测得固体质量随温度的变化如图所示,则乃时所得晶体的化学式为 ,请写出简要的解题过程。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
碳酸锂广泛应用与陶瓷和医药等领域,以锂辉石(主要成分为LiAlSi2O6)为原材料制备Li2CO3的工艺流程如下:
已知:①2LiAlSi2O6+H2SO4(浓)  Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓
②Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的PH分别为3.2、4.7、9.0和11.1
③某些物质的溶解度(S)如右表
请回答下列问题:
(1)锂辉石用浓硫酸浸取之前要粉碎成细颗粒的目的是 。
(2)滤液a中含有Li+、SO42-,另含有Fe3+、Al3+、Fe2+、Mg2+ 、Ca2+、Na+等杂质,步骤Ⅱ需在搅拌下加入石灰石以调节溶液的pH到6.0~6.5,此时沉淀的杂质离子有 。
(3)步骤Ⅱ在滤液a中加入的除杂剂依次为适量的H2O2溶液,石灰乳和Na2CO3溶液,发生反应的离子方程式有 。
(4)步骤Ⅲ中加入饱和Na2CO3溶液过滤后需要用热水洗涤的原因是 。
(5)从滤液c中可回收的主要物质是 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
工业上用重晶石(BaSO4)制备BaCO3的常用方法主要有高温锻烧还原法、沉淀转化法等。高温煅烧还原法的工艺流程可简单的表示如下:
(1)若“煅烧”时产生一种有毒的还原性气体,则反应的化学方程式为______。
(2)工业上煅烧重晶石矿粉时,为使BaSO4得到充分的还原和维持及应所需的高温,应采取的措施是______。
a.加人过量的炭,同时通入空气 b.设法将生成的BaS及时移出
(3)在第一次过滤后洗涤,检验是否洗涤干净的试剂最好是______。
(4)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:
BaSO4 (s)+CO32-(aq) BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)
则:①在实验室将少量BaSO4固体全部转化为BaCO3的实验操作方法与步骤为______。
②与高温煅烧还原法相比,沉淀转化法的优点主要有______。
③已知:Ksp(BaCO3)=2.40×10-9,Ksp(BaSO4)=1.20×10-10。现欲用沉淀转化法将BaSO4转化为BaCO3,该反应的平衡常数为______。如用1.00 L 0. 210 mol ? L-1 Na2CO3溶液处理,试计算BaSO4被转化的质量______(要有计算过程,结果保留3位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com