


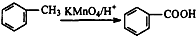
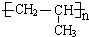 ��
�� ��
�� ��
�� ��
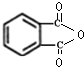
�� ���� ��A������ͼ��������Է�������Ϊ42�����������̼ԭ����Ϊ$\frac{42}{12}$=3��6����A�ķ���ʽΪC3H6��������ױ��������к���̼̼˫������AΪCH3CH=CH2��A������Ϣ��ȩ�ļӳɷ�Ӧ����B��B�ܷ���������Ӧ�����B�����������ӳɷ�Ӧ����C���л���C�ĺ˴Ź���������ʾ������к���5�ֻ�ѧ������ͬ����ԭ�ӣ��Ҹ���֮��Ϊ3��2��2��2��1����BΪCH3CH2CH2CHO��CΪCH3CH2CH2CH2OH���ڶ��ױ�����������Ӧ����DΪ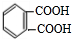 ��C��D����������Ӧ����DBPΪ
��C��D����������Ӧ����DBPΪ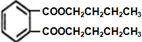 ���ݴ˽��
���ݴ˽��
��� �⣺��A������ͼ��������Է�������Ϊ42�����������̼ԭ����Ϊ$\frac{42}{12}$=3��6����A�ķ���ʽΪC3H6��������ױ��������к���̼̼˫������AΪCH3CH=CH2��A������Ϣ��ȩ�ļӳɷ�Ӧ����B��B�ܷ���������Ӧ�����B�����������ӳɷ�Ӧ����C���л���C�ĺ˴Ź���������ʾ������к���5�ֻ�ѧ������ͬ����ԭ�ӣ��Ҹ���֮��Ϊ3��2��2��2��1����BΪCH3CH2CH2CHO��CΪCH3CH2CH2CH2OH���ڶ��ױ�����������Ӧ����DΪ ��C��D����������Ӧ����DBPΪ
��C��D����������Ӧ����DBPΪ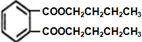 ��
��
��1��������������֪��A�Ľṹ��ʽΪCH3CH=CH2��CH3CH=CH2��һ�������·����Ӿ۷�Ӧ���ɾ۱�ϩ���۱�ϩ�Ľṹ��ʽ��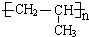 ����Ӧ����ʽΪ��n CH3CH=CH2 $\stackrel{������}{��}$
����Ӧ����ʽΪ��n CH3CH=CH2 $\stackrel{������}{��}$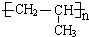 ��
��
�ʴ�Ϊ��CH3CH=CH2��n CH3CH=CH2 $\stackrel{������}{��}$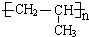 ��
��
��2��DΪ ��D�еĺ������������Ȼ����л���D�������л���C��Ӧ����DBP�ķ�Ӧ��CH3CH2CH2CH2OH���ڱ������ᷢ��������Ӧ����Ӧ�ķ���ʽΪ��
��D�еĺ������������Ȼ����л���D�������л���C��Ӧ����DBP�ķ�Ӧ��CH3CH2CH2CH2OH���ڱ������ᷢ��������Ӧ����Ӧ�ķ���ʽΪ�� ��
��
�ʴ�Ϊ���Ȼ��� ��
��
��3��A��AΪCH3CH=CH2������̼̼˫�����ܷ����ۺϷ�Ӧ���ӳɷ�Ӧ��������Ӧ����A��ȷ��
B��CΪCH3CH2CH2CH2OH����C��Ϊͬ���칹�壬�Һ�����ͬ�����ŵ��л�����CH3CH2CH��OH��CH3����CH3��2C��OH��CH3�֡���CH3��2CHCH2��OH��3�֣���B����
C����Ϊ�������м����ܱ����Ը���������������ڶ��ױ�����������D������˵���л�������л���֮�����Ӱ�죬��C��ȷ��
D��1mol DBP���뺬2mol NaOH����Һ��ȫ��Ӧ����D����
��ѡ��AC��
��4���ٸ����м����+C$��_{��}^{Ũ����}$DBP+H2O�����м����Ϊ�� ���ָ���E+C$��_{��}^{Ũ����}$�м�����Լ�E��C8H4O3������EΪ��
���ָ���E+C$��_{��}^{Ũ����}$�м�����Լ�E��C8H4O3������EΪ�� ��
��
�ʴ�Ϊ�� ��
��
�ڹ�ҵ�������л���E�ķ�Ӧ���£�2X+9O2$��_{390��}^{����}$2E+4CO2+4H2O��������X��һ�����ֻ�����֣����ݷ�Ӧǰ��ԭ���غ㣬�����Ƴ�X�ķ���ʽ��C10H8���ṹ��ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶϣ�ע������л������ʽ����Ӧ�����Լ���Ŀ����ķ�Ӧ��Ϣ�����ƶϣ������л��������������ת���ǹؼ����Ѷ��еȣ�


 ����ν����Ž̲��㽭���̴�ѧ������ϵ�д�
����ν����Ž̲��㽭���̴�ѧ������ϵ�д� �����Ļ������������������ϵ�д�
�����Ļ������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 20 | 40 | 60 | 80 |
| �ܽ�ȣ�Li2CO3��/g | 1.33 | 1.17 | 1.01 | 0.85 |
| �ܽ�ȣ�Li2SO4��/g | 34.2 | 32.8 | 31.9 | 30.7 |
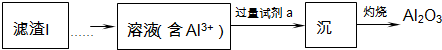
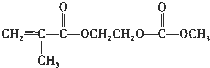 ��д���õ�������������������Һ��Ӧ�Ļ�ѧ����ʽ��
��д���õ�������������������Һ��Ӧ�Ļ�ѧ����ʽ��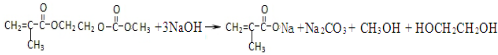 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
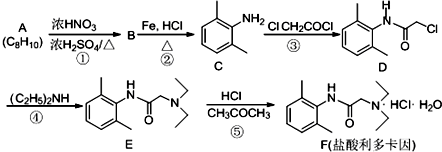

 ����Ӧ����Ϊȡ����Ӧ�����������У���Ӧ���������ͬ�Ļ��Тۢܣ��Ӧ��ţ���
����Ӧ����Ϊȡ����Ӧ�����������У���Ӧ���������ͬ�Ļ��Тۢܣ��Ӧ��ţ��� ��RΪ������
��RΪ������ ��д�ṹ��ʽ����
��д�ṹ��ʽ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

 ��
��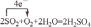 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
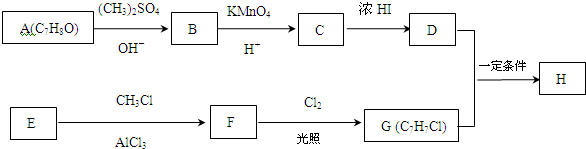


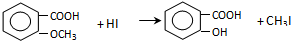 ��
��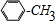 +Cl2$\stackrel{����}{��}$
+Cl2$\stackrel{����}{��}$ +HCl����Ӧ����Ϊȡ����Ӧ��
+HCl����Ӧ����Ϊȡ����Ӧ��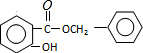 ��
��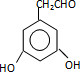 ����
����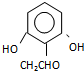 ������дһ�ּ��ɣ�
������дһ�ּ��ɣ� 
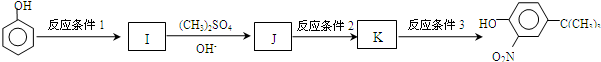
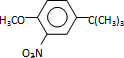 ����Ӧ����3���õ��Լ�ΪŨHI��
����Ӧ����3���õ��Լ�ΪŨHI���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
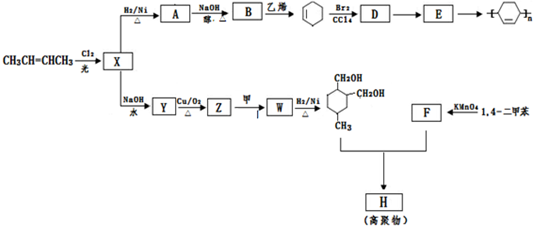
 ��
�� �����
����д��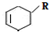 R����ȡ�������⣩
R����ȡ�������⣩ ��
��
 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ijͬѧ�������ͼ��ʵ�飺
ijͬѧ�������ͼ��ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Al3+��Cl-��OH-��5��2��4��4�� | B�� | NH4+��Ba2+��OH-��Cl-��1��1��1��2�� | ||
| C�� | Fe3+��Na+��Cl-��S2-��1��2��3��1�� | D�� | K+��H+��I-��NO3-��1��1��1��1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 N2H4���£���������ҩ��ԭ�ϣ�Ҳ���������ȼ�ϣ���1���������ᷴӦ��N2H6Cl2��Һ�������ԣ���ˮ�д������·�Ӧ��
N2H4���£���������ҩ��ԭ�ϣ�Ҳ���������ȼ�ϣ���1���������ᷴӦ��N2H6Cl2��Һ�������ԣ���ˮ�д������·�Ӧ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com