
| A、全部为Al(OH)3沉淀 |
| B、几乎全部以[Al(OH)4]-形式存在于溶液中 |
| C、一部分为Al(OH)3沉淀,一部分以Al3+存在于溶液中 |
| D、一部分为Al(OH)3沉淀,一部分以[Al(OH)4]-形式存在于溶液中 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、R在元素周期表中位置为第四周期VIII族 |
| B、Na2RO4水溶液可以用于杀菌消毒和净水 |
| C、1molY或Z与足量的R反应均转移2mol电子 |
| D、G为极性分子,中心原子采取sp2杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、淀粉
| ||||
B、纤维素
| ||||
C、油脂
| ||||
D、蛋白质
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液态HCl不导电,所以HCl不是电解质 |
| B、NH3溶于水形成的溶液能导电,所以NH3是电解质 |
| C、电解质一定能导电,能导电的物质一定属于电解质 |
| D、AgCl在水溶液中难导电,但熔融状态下能导电,所以AgCl是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、装置①中K键闭合时,片刻后CuSO4溶液中c(Cl-)增大 |
| B、装置①中K键闭合时,片刻后可观察到滤纸a点变红色 |
| C、装置②中铁腐蚀的速度由大到小的顺序是:只闭合K1>只闭合K3>只闭合K3>都断开 |
| D、装置③中当铁制品上析出1.6g铜时,电源正极输出的电子数为0.05NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、质量相等、密度不等的N2和C2H4 |
| B、等体积等密度的CO和N2 |
| C、等温等体积的O2和Cl2 |
| D、等压等体积的NH3和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N1:N2=n1:n2=V1:V2 | ||
| B、同温同体积时,等质量的气体P1:P2=M1:M2 | ||
| C、同温同压下,ρ1:ρ2=M2:M1 | ||
D、同温同压下,气体密度ρ=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH |
| △ |
| CO2 |
| NH3,CO2 |
| △ |
| HCl溶液 |
| 石灰乳 |
| 煅烧 |
| A、①③⑤ | B、②③④ |
| C、②④⑤ | D、①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
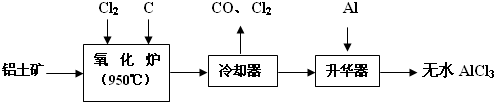
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com