
| A. | 硅相对于氢气便于运输、贮存,从安全角度考虑,硅是有开发价值的燃料 | |
| B. | 硅在地壳中含量居第二位,在地球上有丰富的硅资源,如石英、水晶、玛瑙的主要成分都是单质硅 | |
| C. | 存放NaOH溶液的试剂瓶应用玻璃塞 | |
| D. | 二氧化硅是一种良好的半导体材料 |
分析 A.硅常温下为固体,性质较稳定,便于贮存,较为安全,硅是有开发价值的燃料;
B.石英、水晶、玛瑙主要成分是二氧化硅;
C.二氧化硅能够与氢氧化钠反应生成硅酸钠和水;
D.二氧化硅不导电.
解答 解:A.硅常温下为固体,性质较稳定,便于贮存,较为安全,硅是有开发价值的燃料,故A正确;
B.硅在地壳中含量居第二位,在地球上有丰富的硅资源,如石英、水晶、玛瑙的主要成分都是二氧化硅,故B错误;
C.二氧化硅能够与氢氧化钠反应生成硅酸钠和水,硅酸钠具有粘性,所以碱性物质不能用磨口玻璃塞盛放,故C错误;
D.二氧化硅不导电,是绝缘体,故D错误;
故选:A.
点评 本题考查了硅及其化合物性质,熟悉二氧化硅酸性氧化物的性质是解题关键,注意碱性物质保存注意问题,题目难度不大.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:解答题
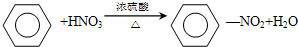 ,该反应的类型是取代反应.
,该反应的类型是取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| B. | 向某溶液中加入氯化钡溶液有白色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液中一定有Ag+ | |
| C. | 向某溶液中先加入盐酸酸化,没有明显现象,再加入BaCl2溶液,有白色沉淀产生,则原溶液中一定有SO42- | |
| D. | 向某溶液中加入加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则原溶液一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/min | 0 | 1 | 2 | 3 | 4 |
| n(H2O)/mol | 1 | 0.8 | 0.65 | 0.6 | 0.6 |
| n(CO)/mol | 0.8 | 0.6 | 0.45 | 0.4 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.该电池电池表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图.该电池电池表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑤ | C. | ③④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.25mol,0.25mol | B. | 0.75mol,0.75mol | C. | 1mol,1mol | D. | 3mol,3mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com