
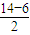 =4,若只含有三键,则分子中含有2个三键.
=4,若只含有三键,则分子中含有2个三键.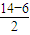 =4,若只含有三键,则分子中含有2个三键,符合条件的结构简式为HC≡C-C≡C-CH2-CH3或HC≡C-CH2-C≡C-CH3或HC≡C-CH2-CH2-C≡CH或CH3-C≡C-C≡C-CH3等,
=4,若只含有三键,则分子中含有2个三键,符合条件的结构简式为HC≡C-C≡C-CH2-CH3或HC≡C-CH2-C≡C-CH3或HC≡C-CH2-CH2-C≡CH或CH3-C≡C-C≡C-CH3等,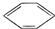 +Br
+Br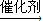
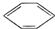 -Br+HBr.
-Br+HBr.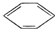 +Br
+Br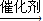
 -Br+HBr;取代反应
-Br+HBr;取代反应

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:







查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 人们对苯的结构及性质的认识经历了一个漫长的过程.
人们对苯的结构及性质的认识经历了一个漫长的过程. +Br
+Br| 催化剂 |
 -Br+HBr
-Br+HBr +Br
+Br| 催化剂 |
 -Br+HBr
-Br+HBr查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com