

 ;
; ;
;
 .
. 分析 A和溴水发生的是加成反应,根据加成产物可判断A的结构简式为CH2=C(CH3)CH2CH3,反应②是水解反应,生成物B的结构简式为CH3CH2C(CH3)OHCH2OH.B氧化得到C,则C的结构简式为CH3CH2C(CH3)OHCOOH;根据C和D的分子式的可判断,反应④是消去反应,即D的结构简式为CH3CH=C(CH3)COOH,反应⑤属于卤代烃的水解反应,则E的结构简式为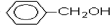 ,E和D通过酯化反应生成F,则F的结构简式为
,E和D通过酯化反应生成F,则F的结构简式为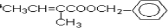 ,结合有机物的结构和性质解答该题.(1)根据烃A的结构简式结合系统命名法命名;
,结合有机物的结构和性质解答该题.(1)根据烃A的结构简式结合系统命名法命名;
(2)根据C的结构简式为CH3CH2C(CH3)OHCOOH书写官能团名称;根据反应⑤推出物质E;
(3)取代反应指有机化合物分子中原子或原子团被其它原子或原子团所代替的反应,结合各反应进行分析;
(4)反应④为CH3CH2C(CH3)OHCOOH在浓硫酸作用下发生消去反应;
(5)E的结构简式为 ,属于芳香族化合物的同分异构体为含有苯环的异构体,据此书写.
,属于芳香族化合物的同分异构体为含有苯环的异构体,据此书写.
解答 解:A和溴水发生的是加成反应,根据加成产物可判断A的结构简式为CH2=C(CH3)CH2CH3,反应①方程式为:CH2=C(CH3)CH2CH3+Br2→CH2BrCBr(CH3)CH2CH3
,反应②是水解反应,方程式为: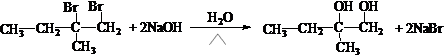 ,生成物B的结构简式为CH3CH2C(CH3)OHCH2OH.B氧化得到C,则C的结构简式为CH3CH2C(CH3)OHCOOH;根据C和D的分子式的可判断,反应④是消去反应,为CH3CH2C(CH3)OHCOOH在浓硫酸作用下发生消去反应,反应的方程式为
,生成物B的结构简式为CH3CH2C(CH3)OHCH2OH.B氧化得到C,则C的结构简式为CH3CH2C(CH3)OHCOOH;根据C和D的分子式的可判断,反应④是消去反应,为CH3CH2C(CH3)OHCOOH在浓硫酸作用下发生消去反应,反应的方程式为 ,即D的结构简式为CH3CH=C(CH3)COOH,反应⑤属于卤代烃的水解反应,反应的方程式为
,即D的结构简式为CH3CH=C(CH3)COOH,反应⑤属于卤代烃的水解反应,反应的方程式为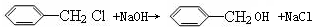 ,则E的结构简式为
,则E的结构简式为 ,E和D通过酯化反应生成F,则F的结构简式为
,E和D通过酯化反应生成F,则F的结构简式为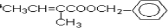 ,反应⑥为酯化反应,反应的方程式为
,反应⑥为酯化反应,反应的方程式为 ,
,
(1)A的结构简式为CH2=C(CH3)CH2CH3,含有碳碳双键为烯烃,主链含有4个碳,双键最近一端为1号,2号碳上有一甲基,所以系统命名法对A物质进行命名为:2-甲基-1-丁烯,
故答案为:2-甲基-1-丁烯;
(2)C的结构简式为CH3CH2C(CH3)OHCOOH,其官能团名称为醇羟基、羧基,反应⑤为氯代烃的水解反应,反应的方程式为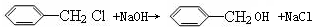 ,E的结构简式为
,E的结构简式为 ,
,
故答案为:羟基、羧基; ;
;
(3)根据官能团的变化可知①为加成反应,②为取代反应,③为氧化反应,④为消去反应,⑤为取代反应,⑥为取代反应,
故答案为:②⑤⑥;
(4)反应④为CH3CH2C(CH3)OHCOOH在浓硫酸作用下发生消去反应,反应的方程式为 ,
,
故答案为: ;
;
(5)E的结构简式为 ,属于芳香族化合物说明含有苯环,E属于芳香族化合物所有的同分异构体为
,属于芳香族化合物说明含有苯环,E属于芳香族化合物所有的同分异构体为
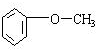 ,
,
故答案为:
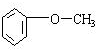 .
.
点评 本题考查有机物的推断,题目难度中等,本题注意从A的结构入手采取正推的方法进行推断,把握官能团的性质以及官能团的转化为解答该题的关键,易错点为同分异构体的判断,注意结合题给信息.


科目:高中化学 来源: 题型:解答题
| 熔点/℃ | 沸点/℃ | 燃烧热/kJ•mol-1 | |
| 铝 | 660 | 2467 | 602 |
| 氧化铝 | 2050 | 2980 | / |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种镇痛和麻醉药物,可由化合物B(
)是一种镇痛和麻醉药物,可由化合物B( )通过以下路线合成得到.
)通过以下路线合成得到.
 .
. +HBr+CH3Br.
+HBr+CH3Br. 等.
等. 所示)的合成路线流程图(无机试剂任选).
所示)的合成路线流程图(无机试剂任选).
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由${\;}_{1}^{2}$H和${\;}_{8}^{18}$O所组成的11g水中所含中子数为6NA | |
| B. | H2O和D2O互称为同素异形体,且两者的化学性质相似 | |
| C. | ${\;}_{8}^{18}$O2和${\;}_{8}^{16}$O3互称为同位素 | |
| D. | 金刚石和石墨互为同素异形体,两者之间的转化属于物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 步骤 | 实验操作 | 预期现象及结论 (步骤1只写现象) |
| 1 | 在A、B两支洁净的试管中各加入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水, 至沉淀恰好溶解,此时制得pH均约为8的银氨溶液. | 先生成白色沉淀,后沉淀溶解. |
| 2 | 往A、B试管加入3滴乙醛,然后在A试管中加1滴NaOH溶液;振荡后将两支试管放在热水浴中温热. | 若A试管比B试管出现的银镜时间短、光亮,则则溶液pH大,反应速率快; 若A试管比B试管出现的银镜时间长,则则溶液pH大,反应速率慢. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 步骤(3)后可以确定CO32-一定不存在 | |
| B. | 忽略步骤(1)对实验结论并无影响 | |
| C. | 不能确定原溶液是否含有K+和Cl- | |
| D. | 若把步骤(2)产生的气体通入步骤(1)的滤液中,又可产生0.78g沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应物 | 催化剂 | 温度 | |
| ① | 10mL10% H2O2溶液 | 无 | 25℃ |
| ② | 10mL20% H2O2溶液 | 无 | 25℃ |
| ③ | 10mL20% H2O2溶液 | 无 | 40℃ |
| ④ | 10mL20% H2O2溶液 | 1~2滴0.1mol/LFeCl3溶液 | 40℃ |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
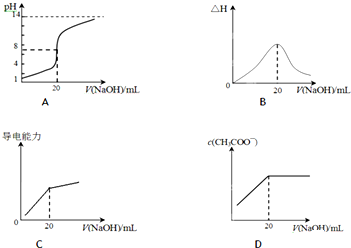 Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.
Ⅰ.常温下,某水溶液中只存在下列四种离子:Na+、A-、H+、OH-,据题意回答下列问题.| 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
| CH3COOH | 1.8×10-5 | HCN | 5×10-10 |
| H2CO3 | Ka1=4.2×10-7 | HClO | 3×10-8 |
| Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
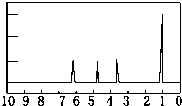 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com