
| A、ns2np3 |
| B、ns2np5 |
| C、ns1 |
| D、ns2np6 |


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、前10min反应的平均速率V(C)=0.10mol/L?min |
| B、10min后向容器中加入A,重新平衡时A的转化率一定大于50% |
| C、恒温下将反应容器体积缩小一半,则D的平衡浓度小于1.0mol/L |
| D、反应达平衡时B的平衡浓度是1.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
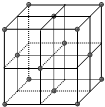 碳有多种同素异形体,常见的有金刚石,石墨,和C60(足球烯)分子,根据报道科研人员应用计算机模拟出结构类似C60的物质N60分子和Si60分子,
碳有多种同素异形体,常见的有金刚石,石墨,和C60(足球烯)分子,根据报道科研人员应用计算机模拟出结构类似C60的物质N60分子和Si60分子,查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | I1 | I2 | I3 | I4 |
| E | 500 | 4600 | 6900 | 9500 |
| F | 740 | 1500 | 7700 | 10500 |
| H | 580 | 1800 | 2700 | 11600 |
| I | 420 | 3100 | 4400 | 5900 |
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | |||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | Na+ Mg2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | OH- CO32- Cl- NO3- SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能层n=3 能级种类d 自旋状态↑ |
| B、能层n=2 能级种类d 自旋状态↓ |
| C、能层n=4 能级种类p 自旋状态↓ |
| D、能层n=3 能级种类p 自旋状态↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、淀粉、纤维素、蛋白质都是天然高分子化合物 |
| B、用于奥运“祥云”火炬的丙烷是一种清洁燃料 |
| C、用大米酿的酒在一定条件下密封保存,时间越长越香醇 |
| D、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com