
����Ŀ�����ڳ����ܽ�ƽ����ܶȻ�����������˵������ȷ����(����)
A. Kspֻ�����ܵ���ʵ����ʺ��¶��йأ�������Һ�е�����Ũ����
B. ������Na2SO4��Һ���뵽����ʯ��ˮ�У��а�ɫ����������˵��Ksp[Ca(OH)2]����Ksp(CaSO4)
C. ��֪25 ��ʱKsp[Fe(OH)3]��4.0��10��38������¶��·�ӦFe(OH)3��3H��![]() Fe3����3H2O��ƽ�ⳣ��K��4.0��104
Fe3����3H2O��ƽ�ⳣ��K��4.0��104
D. ��֪25 ��ʱKsp[Mg(OH)2] ��1.8��10��11����MgCl2��Һ�м��백ˮ�����Һ��pH��11���������������ʱ��Һ�е�c(Mg2��)��1.8��10��5mol��L��1
���𰸡�B
��������
A. Ksp���¶ȵij�����ֻ���¶ȸı���ı䣬��ͬ���ʵ��ܽ�������ͬ�������ʱ����������йأ���A��ȷ��
B. ������Na2SO4��Һ���뵽����ʯ��ˮ�У��а�ɫ����������˵������Ƶ��ܽ��С�����ܶȻ�����ʽ���Ͳ�ͬ������˵����С����B����
C. Ksp[Fe(OH)3]=c3(OH)c(Fe3+)����Ӧ��ƽ�ⳣ��K=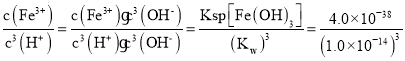 =4.0��104����C��ȷ��
=4.0��104����C��ȷ��
D. ��û��Һ��pH=11��Ksp[Mg(OH)2]=c2(OH)c(Mg2+)��c(OH)=103���������c(Mg2+)=1.8��103mol/L����D��ȷ��
��ѡB��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ĺ����Ƽ�Ĺ�����������ͼ��ʾ������˵����ȷ����
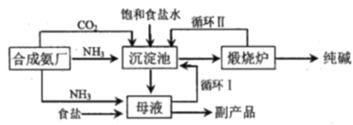
A.��ĸҺ�м���ʳ�ε���ҪĿ����ʹNaHCO3���������
B.��ĸҺ�о���ѭ������������ص���Ҫ��Na2CO3��NH4Cl�Ͱ�ˮ
C.�������з�Ӧ�Ļ�ѧ����ʽ��2NH3+CO2+2NaCl+H2O=2NH4Cl+Na2CO3
D.���ѭ������Ŀ����ʹԭ�϶�����̼�����ʴ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ��������������ȷ����(����)
A. ��������ΪNA�Ķ�������Ͷ�����̼��������к��е�ԭ����Ϊ3NA
B. �κ������£�20 L �������еķ�������������ΪNA
C. �ڱ�״���£�2 g��������NA����ԭ��
D. ���ʵ�����ȵ��κ������ж�������ͬ��ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к���MgCl2���Ӻ�ˮ����ȡþ����ȷ�ķ�����
A.��ˮ![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
B.��ˮ![]() MgCl2��Һ�� MgCl2�����ڣ�
MgCl2��Һ�� MgCl2�����ڣ�![]() Mg
Mg
C.��ˮ![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
D.��ˮ![]() Mg(OH)2
Mg(OH)2![]() MgCl2��Һ �� MgCl2�����ڣ�
MgCl2��Һ �� MgCl2�����ڣ�![]() Mg
Mg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ���ش��������⣺
��1�������������ʣ���KCl�����Һ̬HCl��CO2 �ܹ���CaCO3�����ϡ����߾ƾ�C2H5OH �����ڵ�NaCl ��Ũ��ˮ���������ڵ���ʵ��ǣ�����ţ���ͬ��___________�����ڷǵ���ʵ���____________���ܵ������__________��
��2����֪��2Fe3++2I===2Fe2++I2��2Fe2++Br2===2Fe3++2Br���ں��� FeI2�� FeBr2����Һ��ͨ������ Cl2�������ȱ�������������_____��I��Br��Fe2+��ԭ����ǿ������˳��Ϊ��___________��
��3��ʵ������ʢװNaOH��Һ�Լ�ƿ����Ƥ������ľ���������ò��������û�ѧ����ʽ���ͣ�_________________________________________________
��4�� 0.3mol������0.4mol������̼������֮��___________������������֮��______________������ԭ����֮��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ת����ϵ��

������ͼ��ʵ�����ش��������⣺(����ѧʽ��ʾ)
��1��A��_____��X��ĩ��_______��
��2��д����Ӧ�ٵĻ�ѧ����ʽ___________________��
��3��д����Ӧ�ڵ����ӷ���ʽ___________________��
��4��д����ȥ����C�л��е�NaHCO3�Ļ�ѧ����ʽ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ⱻ��Ϊ������Ԫ����,��ѧ�����ز����ɷ��ε�ȱ����,KI��KIO3���Ⱥ����ڼӵ����С�KI�������ڷ����Լ����й���ϡ���ҩ��,���Ʊ�ԭ������:
��ӦI : 3I2+ 6KOH== KIO3 +5KI+ 3H2O
��ӦII: 3H2S+KIO3=3S��+KI+ 3H2O
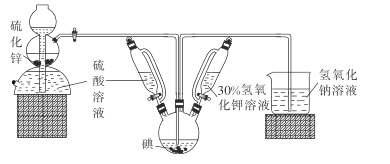
��ش��й����⡣
(1)���շ������з�����Ӧ�Ļ�ѧ����ʽΪ_______��װ����ʢװ30%����������Һ������������_________��
(2)�ر����շ���������,�ȵ���30%��KOH��Һ.���۲쵽������ƿ����Һ��ɫ���ػ�ɫ��Ϊ______(������) ,ֹͣ����KOH��Һ;Ȼ��______(�����),��������ƿ���ձ��в������ݵ����ʽӽ����ʱֹͣͨ����
(3)����������Һ,����������ƿ�е���Һ����ˮԡ����,��Ŀ����_____________��
(4)��������ƿ�е���Һ�����ձ���,����̼�ᱵ,�ڹ������й���,���˵õ��ij����г����й���̼�ᱵ��,���������ᱵ��___________(������)���ϲ���Һ��ϴ��Һ,�����������ᾧ������ó�Ʒ��
(5)ʵ����ģ�ҵ�Ʊ�KIO3��������:
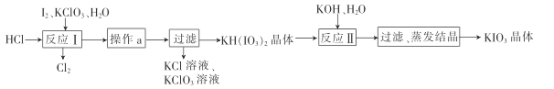
�������ʵ��ܽ�ȼ��±�:
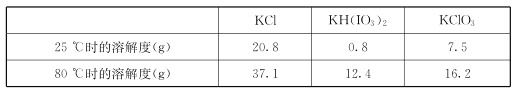
�����ϱ����ݷ�����֪��������a��Ϊ__________________��
���ö��Ե缫���KI��ҺҲ���Ʊ�KIO3,���ⷨ��ȣ����������Ʊ�KIO3��ȱ����____________��
(6)ijͬѧ�ⶨ.��������������KIO3��Ʒ�Ĵ��ȡ�
ȡ1.00 g��Ʒ��������ˮ�в��������ữ���ټ��������KI�������ĵ�����Һ����εμ�2.0 mol��L-1 Na2S2O3 ��Һ,ǡ����ȫ��Ӧʱ������12. 60 mL Na2S2O3��Һ������Ʒ��KIO3����������Ϊ_______(��֪��Ӧ:I2+2Na2S2O3=2NaI+Na2S4O6)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��A 0.2 mol�������г��ȼ�պ����ɻ�����B��C��1.2 mol��������������⣺
��1����A�ķ���ʽΪ____��
��2������A����ʹ��ˮ��ɫ������һ�������£�������������ȡ����Ӧ����һ�ȴ���ֻ��һ�֣������A�Ľṹ��ʽΪ_____��
��3������A��ʹ��ˮ��ɫ���ڴ��������£���H2�ӳɣ���ӳɲ��ᆳ�ⶨ�����к���4��������A���п��ܵĽṹ��ʽ�ֱ�Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2L�����ܱ�������Ͷ��һ������A��B������Ӧ��3A(g)+bB(g)cC(g) ��H=QkJmol1(Q��0)��12sʱ����C�����ʵ���Ϊ0.8mol(��Ӧ������ͼ��ʾ)������˵������ȷ����(����)
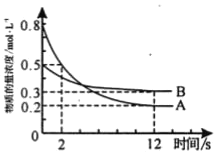
A. ͼ�н���ʱA���������ʵ���A����������
B. 0-2s�ڣ���A��ʾ�ķ�Ӧ����Ϊ0.15molL1s1
C. ��ѧ������֮��b��c=1��4
D. 12s�ڣ���Ӧ�ų�0.2Q kJ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com