
NA代表阿伏加德罗常数,下列说法正确的是
A. 在常温常压下,28gN2与CO混合物气体中所含的分子数目一定为NA
B. 标准状况下,17g氨气所含原子数目为NA
C. 在常温常压下,11.2L氮气所含的原子数目为NA
D. NA个氢分子所占有的体积一定为22.4L
科目:高中化学 来源:2016-2017学年浙江省台州市高二上学期期末质量评估考试化学试卷(解析版) 题型:推断题
4-乙氧基乙酰乙酰苯胺(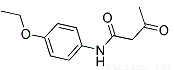 ),简称AAPP,常用作染料、有机颜料中间体。其合成路线如下:
),简称AAPP,常用作染料、有机颜料中间体。其合成路线如下:
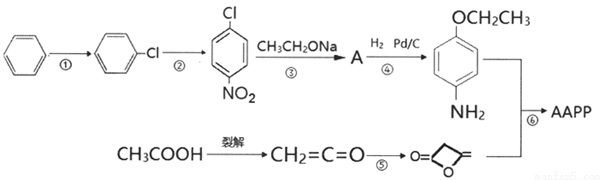
已知: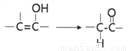
回答下列问题:
(1)下列有关说法正确的是_________
A.反应③是取代反应,反应⑤是加成反应
B.1mol苯完全燃烧需要6molO2
C.CH3COOH不能与新制Cu(OH)2浊液反应
D.CH2=C=O在一定条件下能生成乙醇
(2)反应②的反应条件是_________
(3)A的结构简式_________
(4)反应⑥的化学方程式_________
(5)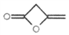 有多种同分异构体,写出三种符合下列要求的同分异构体_________
有多种同分异构体,写出三种符合下列要求的同分异构体_________
a.链状化合物 b.能发生银镜反应,但不能在稀硫酸中水解 c.不能与Na反应
查看答案和解析>>
科目:高中化学 来源:2017届天津市红桥区高三上学期期末考试(下学期开学考试)化学试卷(解析版) 题型:选择题
有关下列四个常用电化学装置的叙述中,正确的是

A. Ⅰ所示电池中,MnO2的作用是催化剂
B. Ⅱ所示电池放电过程中,硫酸浓度不断增大
C. Ⅲ所示装置工作过程中,严桥K+移向硫酸锌溶液
D. Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宿州市高一上学期期末教学质量检测(a卷)化学试卷(解析版) 题型:选择题
某200mLFe2(SO4)3溶液中含有0.1molFe3+,该溶液中SO42-的物质的量浓度为
A. 0.75mol/L B. 0.5mol/L C. 1mol/L D. 0.25mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宿州市高一上学期期末教学质量检测(a卷)化学试卷(解析版) 题型:选择题
下列关于浓硫酸与浓硝酸的叙述不正确的是
A. 敞口久置,二者浓度均会变小 B. 常温下,均会使铝、铁钝化
C. 敞口久置,二者质量均会变大 D. 均具有强氧化性
查看答案和解析>>
科目:高中化学 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:简答题
碘及其化合物在生活中应用广泛。含有碘离子的溶液需回收处理。
(1)“硫碘循环”法是分解水制备氢气的研究热点,涉及下列两个反应:
反应Ⅰ:SO2(g)+I2(aq)+2H2O(l)=2HI(aq)+H2SO4(aq) △H1
反应Ⅱ:HI(aq)=1/2H2(g)+1/2I2(aq) △H2
①反应:SO2(g)+2H2O(1)=H2SO4(aq)+H2(g)的△H=_________(用△H1、△H2表示)。
②反应I发生时,溶液中存在如下平衡:I2(aq)+I-(aq)  I3-(aq),其反应速率极快且平衡常数大。现将1mol SO2缓缓通入含1mol I2的水溶液中至恰好完全反应。溶液中I3-的物质的量[n(I3-)]随反应时间(t)的变化曲线如图1所示。开始阶段。N(I3-)逐渐增大的原因是_______________。
I3-(aq),其反应速率极快且平衡常数大。现将1mol SO2缓缓通入含1mol I2的水溶液中至恰好完全反应。溶液中I3-的物质的量[n(I3-)]随反应时间(t)的变化曲线如图1所示。开始阶段。N(I3-)逐渐增大的原因是_______________。

(2)用海带提取碘时,需用氯气将碘离子氧化成单质。酸性条件下,若氯气过量就能将碘单质进一步氧化成碘酸根离子,写出氯气与碘单质反应的离子方程式:____________。
(3)科研小组用新型材料Ag/TiO2对溶液中碘离子进行吸附研究。如图2是不同PH条件下,碘离子吸附效果的变化曲线。据此推断Ag/TiO2材料最适合吸附____(填“酸性”“中性”或“碱性”)溶液中的I-。
(4)氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为I-(aq)+AgCl(s)
 AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=________[用c(Cl-)、Kap(AgCl)和Kaq(AgI)表示]。该方法去除碘离子的原理是________________。
AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=________[用c(Cl-)、Kap(AgCl)和Kaq(AgI)表示]。该方法去除碘离子的原理是________________。
查看答案和解析>>
科目:高中化学 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:选择题
下列实验方案能达到实验目的的是
A. 证明浓度的的改变可导致平衡移动:将少量KCl晶体加入FeCl3+3KSCN Fe(SCN)3+3KCl的平衡体系中
Fe(SCN)3+3KCl的平衡体系中
B. 除去MgCl2溶液中少量的FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量的Mg(OH)2粉末,搅拌一段时间后过滤
C. 检验某溶液中是否含有乙醛:向盛有2mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热
D. 证明Fe3+的氧化性大于I2:将KI溶液和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高一下学期期初化学试卷(解析版) 题型:选择题
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气
体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A. 60 mL B. 45 mL C. 30 mL D. 15 mL
查看答案和解析>>
科目:高中化学 来源:河北省2016-2017学年高一下学期开学考试化学试卷 题型:计算题
取50mL的Na2CO3和Na2SO4 的混合溶液,加入适量Ba(OH)2溶液50mL后,恰好完全反应,过滤得到滤液和12.54g白色沉淀(干燥后),再用足量的稀硝酸处理沉淀,最后沉淀减少到4.66g,并有气体放出。
(1)4.66g白色沉淀是_________(填化学式),写出12.54g白色沉淀加入稀硝酸后变为4.66g所发生反应的离子方程式___________________________;
(2)产生的气体在标准状况下的体积为__________ml;
(3)原混合液中Na2SO4的物质的量浓度______;
(4)计算过滤出12.54g沉淀后,所得滤液中溶质的物质的量浓度(忽略混合溶液体积的变化)______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com