
)已知化合物A、B、M、N含有同一种元素,且A与B,M与N的元素组成相同,A与B在常温下均呈液态。D为固体单质,与X的浓溶液在常温下作用无明显现象,加热时有大量气体产生。(相关转化中所有反应物与生成物均已标出)

(1)若D与E溶液能够发生化合反应。且溶液在反应前后颜色有变化。
①A的电子式为________。D的化学式为________。
②M与E溶液可发生反应生成X,其离子方程式为
_________________________________________________________________
________________________________________________________________。
(2)若D为常见的红色金属单质。用情性电极电解100 mL 0.05 moL·L-1E溶液,导线中通过0.08 mol电子,阳极析出的气体体积为________mL(标准状况),假设溶液体积不变,则所得溶液pH=________。
(3)若D为短周期元素形成的黑色固体单质。反应④的化学方程式为________________________________________________________________。
(4)已知下列几种试剂:
a.无水CuSO4 b.品红溶液 c.酸性KMnO4溶液
d.澄清石灰水 e.饱和NaOH溶液
为了检验(3)中D与X生成的混合气体的成分,某学生用上述试剂(或部分试剂)设计了几种实验方案,下列试剂使用顺序最合理的是________(填序号)。
A.abebd B.adebC.abcbd D.abd
(1)① Fe ②2Fe3++SO2+2H2O===2Fe2++SO42—+4H+ (2)448 1
Fe ②2Fe3++SO2+2H2O===2Fe2++SO42—+4H+ (2)448 1
(3)C+2H2SO4(浓)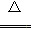 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(4)C
【解析】 本题以框图推断为载体,主要考查了硫、铁及其化合物的性质,意在考查考生的推断能力及实验能力。(1)A、B均为液体,且组成相同,可能是H2O和H2O2,H2O2在MnO2催化下可分解生成水和O2,故A为H2O2,B为H2O,C为O2;固体单质D与X的浓溶液在常温下不反应,加热时反应生成M、E和H2O,M能与O2反应,D与E溶液能够发生化合反应,且反应前后溶液颜色有变化,则D为Fe,M为SO2,E为Fe2(SO4)3,N为SO3,X为H2SO4。①H2O2中O为-1价,氧原子之间共用一对电子,电子式为 。②SO2具有还原性,Fe3+具有较强的氧化性,SO2在水溶液中可被Fe3+氧化成硫酸。(2)若D为红色单质,则D为Cu,Cu与浓硫酸反应得到的E为CuSO4,用惰性电极电解硫酸铜溶液过程中,阳极生成O2,导线中通过0.08 mol电子时,阳极共生成0.02 mol O2,其体积在标准状况下为448 mL。原溶液中n(CuSO4)=0.1 L×0.05 mol·L-1=0.005 mol,若Cu2+完全反应,转移电子0.005 mol×2=0.01 mol,而实际转移电子为0.08 mol,则说明还存在水的电解,故硫酸铜经电解后完全转化为H2SO4,则c(H+)=2c(CuSO4)=2×0.05 mol·L-1=0.1 mol·L-1,故pH=1。(3)短周期元素中能形成黑色固体单质的是碳,碳与浓硫酸在加热条件下可反应生成CO2、SO2和水。(4)SO2、CO2均是酸性氧化物,与碱反应的现象相似;但SO2具有漂白性和还原性,故可用品红溶液检验SO2,然后用酸性高锰酸钾溶液除去SO2,再用品红溶液检验SO2是否除尽,最后用澄清石灰水检验CO2。由于检验SO2和CO2的试剂均是水溶液,故需首先用无水CuSO4检验产物中的水蒸气,合理的选项为C。
。②SO2具有还原性,Fe3+具有较强的氧化性,SO2在水溶液中可被Fe3+氧化成硫酸。(2)若D为红色单质,则D为Cu,Cu与浓硫酸反应得到的E为CuSO4,用惰性电极电解硫酸铜溶液过程中,阳极生成O2,导线中通过0.08 mol电子时,阳极共生成0.02 mol O2,其体积在标准状况下为448 mL。原溶液中n(CuSO4)=0.1 L×0.05 mol·L-1=0.005 mol,若Cu2+完全反应,转移电子0.005 mol×2=0.01 mol,而实际转移电子为0.08 mol,则说明还存在水的电解,故硫酸铜经电解后完全转化为H2SO4,则c(H+)=2c(CuSO4)=2×0.05 mol·L-1=0.1 mol·L-1,故pH=1。(3)短周期元素中能形成黑色固体单质的是碳,碳与浓硫酸在加热条件下可反应生成CO2、SO2和水。(4)SO2、CO2均是酸性氧化物,与碱反应的现象相似;但SO2具有漂白性和还原性,故可用品红溶液检验SO2,然后用酸性高锰酸钾溶液除去SO2,再用品红溶液检验SO2是否除尽,最后用澄清石灰水检验CO2。由于检验SO2和CO2的试剂均是水溶液,故需首先用无水CuSO4检验产物中的水蒸气,合理的选项为C。


科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题2常用化学计量--物质的量练习卷(解析版) 题型:选择题
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为( )。
A.3.2 g B.4.0 g C.4.2 g D.4.6 g
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题12化学实验基础练习卷(解析版) 题型:选择题
下列关于溶液中所含离子的检验结论正确的是( )。
A.加入氨水时生成白色沉淀,当氨水过量时白色沉淀消失,则原溶液中一定有Al3+存在
B.欲鉴别FeCl2溶液、AlCl3溶液和AgNO3溶液,向3种待测液中分别滴加足量氨水
C.加入盐酸,有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO32—存在
D.加入BaCl2溶液生成白色沉淀,再加足量盐酸沉淀不溶解,则原溶液中一定有SO42—存在
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题11有机化学基础练习卷(解析版) 题型:填空题
Ⅰ是重要的化工原料,可发生下列反应生成Ⅲ和Ⅳ。

化合物Ⅰ可用石油裂解气中的2-戊烯来合成,流程如下:
CH3—CH==CH—CH2—CH3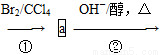 CH2==CH—CH==CH—CH3
CH2==CH—CH==CH—CH3
(1)a的结构简式是________________;②的反应类型是____________。
(2)写出反应①的化学方程式________________,该反应类型是________。
(3)①用甲醇与某有机物发生酯化反应可合成化合物Ⅱ,写出该反应的化学方程式________________________________________________________。
②化合物Ⅱ与新制的氢氧化铜悬浊液反应的化学反应方程式为___________。
(4)化合物Ⅳ是Ⅲ的同分异构体,也有同样的六元环,Ⅳ的结构简式为______。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题11有机化学基础练习卷(解析版) 题型:选择题
下列说法正确的是( )。
A.溴乙烷和甲醇都能发生消去反应
B.乙烯和苯都能与酸性KMnO4溶液发生反应
C.糖类和蛋白质都是人体需要的营养物质
D.纤维素和油脂的水解产物都是葡萄糖
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题10常见非金属元素及其重要化合物练习卷(解析版) 题型:选择题
下列与实验相关的叙述正确的是( )。
A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B.将SO2和Cl2按等物质的量比通入品红溶液中,品红很快褪色
C.NO2与H2O反应的过程中,被氧化的氮原子与被还原的氮原子的个数比为2∶1
D.检验某溶液是否含有SO42—时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮冲刺非选择题增分专练 综合实验设计练习卷(解析版) 题型:实验题
某研究小组利用如图装置探究温度对CO还原Fe2O3的影响(固定装置略)。

(1)MgCO3的分解产物为________。
(2)装置C的作用是_____________________________________________________,
处理尾气的方法为_______________________________________________________。
(3)将研究小组分为两组,按如图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物)。两组分别用产物进行以下实验:
(已知:Fe2+与K3[Fe(CN)6]反应产生蓝色沉淀)。
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是________。
②甲组步骤1中反应的离子方程式为__________________________________________。
③乙组步骤4中,溶液变红的原因为_______________________________________,
溶液褪色可能的原因及其验证方法为______________________________________
④从实验安全考虑,题图装置还可采取的改进措施是__________________________
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮冲刺非选择题增分专练 基本概念、基本理论练习卷(解析版) 题型:填空题
煤直接燃烧的能量利用率较低,为提高其利用率,工业上将煤气化(转变成CO和H2)后再合成乙醇、二甲醚等多种能源。
(1)如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。该电池的负极反应式为______________________。

(2)煤气化所得气体可用于工业合成二甲醚,其反应如下:
2CO(g)+4H2(g) CH3OCH3(g)+H2O(g)。
CH3OCH3(g)+H2O(g)。
同时发生副反应:CO(g)+2H2(g) CH3OH(g);CO(g)+H2O(g)??CO2(g)+H2(g)。
CH3OH(g);CO(g)+H2O(g)??CO2(g)+H2(g)。
在温度为250 ℃、压强为3.0 MPa时,某工厂按投料比V(H2)∶V(CO) =a进行生产,平衡时反应体系中各组分的体积分数如下表:
物质 | H2 | CO | CO2 | (CH3)2O | CH3OH(g) | H2O(g) |
体积分数 | 0.54 | 0.045 | 0.18 | 0.18 | 0.015 | 0.03 |
①投料比a=________;
②250℃时反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数K=________。
CO2(g)+H2(g)的平衡常数K=________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮专题复习 离子反应、氧化还原反应练习卷(解析版) 题型:填空题
亚硝酸(HNO2)是一种与醋酸酸性相当的弱酸,很不稳定,通常在室温下立即分解。
(1)写出亚硝酸的电离方程式: 。
(2)在酸性条件下,当NaNO2与KI按物质的量之比1∶1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为 (填化学式)。
(3)要得到稳定的HNO2溶液,可以向冷冻的NaNO2浓溶液中加入或通入某种物质,下列物质不适合的是 (填字母)。
a.稀硫酸 b.二氧化碳 c.二氧化硫 d.磷酸
(4)碱性工业废水中的N 可用铝粉除去。已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3·H2O、H2O六种物质。
可用铝粉除去。已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3·H2O、H2O六种物质。
①写出上述反应的离子方程式: 。
②发生上述反应后废水的pH将 (填“增大”“减小”或“不变”)。
(5)酸性工业废水中的N 可用尿素除去。尿素
可用尿素除去。尿素
( )与N
)与N 在酸性条件下反应生成两种无毒气体。该反应中生成16.8 L(已折算为标准状况)混合气体时,消耗尿素的质量为 g。
在酸性条件下反应生成两种无毒气体。该反应中生成16.8 L(已折算为标准状况)混合气体时,消耗尿素的质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com