
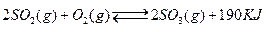
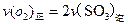 b£®ČŻĘ÷ÖŠĘųĢåµÄĘ½¾ł·Ö×ÓĮæ²»Ėꏱ¼ä¶ų±ä»Æ
b£®ČŻĘ÷ÖŠĘųĢåµÄĘ½¾ł·Ö×ÓĮæ²»Ėꏱ¼ä¶ų±ä»Æ 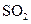 ŗĶ0.10mol
ŗĶ0.10mol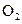 £¬°ė·ÖÖÓŗó“ļµ½Ę½ŗā£¬²āµĆČŻĘ÷ÖŠŗ¬
£¬°ė·ÖÖÓŗó“ļµ½Ę½ŗā£¬²āµĆČŻĘ÷ÖŠŗ¬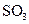 0.18mol£¬Ōņ
0.18mol£¬Ōņ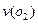 =______
=______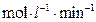 £ŗČō¼ĢŠųĶØČė0.20mol
£ŗČō¼ĢŠųĶØČė0.20mol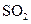 ŗĶ0.10mol
ŗĶ0.10mol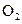 £¬ŌņĘ½ŗā______ŅʶÆ(Ģī”°ĻņÕż·“Ó¦·½Ļņ”±”¢”°ĻņÄę·“Ó¦·½Ļņ”± »ņ”°²»”±)£¬ŌŁ“Ī“ļµ½Ę½ŗāŗó£¬______ mol<n(
£¬ŌņĘ½ŗā______ŅʶÆ(Ģī”°ĻņÕż·“Ó¦·½Ļņ”±”¢”°ĻņÄę·“Ó¦·½Ļņ”± »ņ”°²»”±)£¬ŌŁ“Ī“ļµ½Ę½ŗāŗó£¬______ mol<n(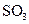 )<______mol”£
)<______mol”£ ½ĢѧĮ·ŠĀĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
½ĢѧĮ·ŠĀĶ¬²½Į·Ļ°ĻµĮŠ“š°ø æĪĒ°æĪŗóĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
æĪĒ°æĪŗóĶ¬²½Į·Ļ°ĻµĮŠ“š°ø æĪĢĆŠ”×÷ŅµĻµĮŠ“š°ø
æĪĢĆŠ”×÷ŅµĻµĮŠ“š°ø »ĘøŌŠ”דŌŖæŚĖćĖŁĖćĮ·Ļ°²įĻµĮŠ“š°ø
»ĘøŌŠ”דŌŖæŚĖćĖŁĖćĮ·Ļ°²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 2SO3(g)ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗā£¬²āµĆc(SO3)£½0.040 mol/L”£ŌņøĆĢõ¼žĻĀ·“Ó¦µÄĘ½ŗā³£ŹżK= £¬SO2µÄĘ½ŗā×Ŗ»ÆĀŹ= ”£
2SO3(g)ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗā£¬²āµĆc(SO3)£½0.040 mol/L”£ŌņøĆĢõ¼žĻĀ·“Ó¦µÄĘ½ŗā³£ŹżK= £¬SO2µÄĘ½ŗā×Ŗ»ÆĀŹ= ”£| A£®ÉżøßĪĀ¶Č | B£®½µµĶĪĀ¶Č | C£®Ōö“óŃ¹Ēæ |
| D£®¼õŠ”Ń¹Ēæ (E)¼ÓČė“߻ƼĮ (G)ŅĘ³öŃõĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā

 2NH3 (g) ¦¤H£½£92.2kJ”¤mol£1
2NH3 (g) ¦¤H£½£92.2kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ČŪµć±ČÉśĢśµĶ |
| B£®ÓėĻąĶ¬ÅØ¶ČµÄŃĪĖį·“Ӧɜ³ÉĒāĘųµÄĖŁĀŹ±ČÉśĢśµÄæģ |
| C£®ŌŚ³±ŹŖµÄæÕĘųÖŠ±ČÉśĢśČŻŅ×±»øÆŹ“ |
| D£®ŌŚĄäµÄÅØĻõĖįÖŠæɶŪ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 FeO(s)+CO(g)µÄĘ½ŗā³£ŹżĪŖK1”£
FeO(s)+CO(g)µÄĘ½ŗā³£ŹżĪŖK1”£ FeO(s)+H2(g)µÄĘ½ŗā³£ŹżĪŖK2£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬ K1”¢K2µÄÖµČēĻĀ£ŗ
FeO(s)+H2(g)µÄĘ½ŗā³£ŹżĪŖK2£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬ K1”¢K2µÄÖµČēĻĀ£ŗ| T(K) | K1 | K2 |
| 973 | 1.47 | 2.36 |
| 1173 | 2.15 | 1.67 |
 CO(g) +H2O(g);”÷H>0£¬ÕāŹĒŅ»øö £ØĢī”°Īü”±»ņ”°·Å”±£© ČČ·“Ó¦£¬ŅŖŹ¹·“Ó¦¢ŪŌŚŅ»¶ØĢõ¼žĻĀ½ØĮ¢µÄĘ½ŗāĻņÓŅŅĘ¶Æ£¬æɲÉČ”µÄ“ėŹ©µÄÓŠ ”£
CO(g) +H2O(g);”÷H>0£¬ÕāŹĒŅ»øö £ØĢī”°Īü”±»ņ”°·Å”±£© ČČ·“Ó¦£¬ŅŖŹ¹·“Ó¦¢ŪŌŚŅ»¶ØĢõ¼žĻĀ½ØĮ¢µÄĘ½ŗāĻņÓŅŅĘ¶Æ£¬æɲÉČ”µÄ“ėŹ©µÄÓŠ ”£ FeO(s)+CO(g)ŌŚĪĀ¶ČT1ĻĀ½ųŠŠ£»Fe(s)+H2O(g)
FeO(s)+CO(g)ŌŚĪĀ¶ČT1ĻĀ½ųŠŠ£»Fe(s)+H2O(g)  FeO(s)+H2(g)ŌŚĪĀ¶ČT2ĻĀ½ųŠŠ£¬ŅŃÖŖT1>T2£¬ĒŅc(CO2)>c(CO)£ØĘäĖūĢõ¼ž¾łĻąĶ¬£©£¬ŌņĮ½Õߵķ“Ó¦ĖŁĀŹ £ØĢīŠņŗÅ£©”£
FeO(s)+H2(g)ŌŚĪĀ¶ČT2ĻĀ½ųŠŠ£¬ŅŃÖŖT1>T2£¬ĒŅc(CO2)>c(CO)£ØĘäĖūĢõ¼ž¾łĻąĶ¬£©£¬ŌņĮ½Õߵķ“Ó¦ĖŁĀŹ £ØĢīŠņŗÅ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 2C(g)“ļµ½»ÆŃ§Ę½ŗāŹ±£ŗ
2C(g)“ļµ½»ÆŃ§Ę½ŗāŹ±£ŗ x C(g)Ę½ŗāŹ±A”¢B”¢CµÄĪļÖŹµÄĮæÖ®±ČĪŖ1
x C(g)Ę½ŗāŹ±A”¢B”¢CµÄĪļÖŹµÄĮæÖ®±ČĪŖ1 ”Ć3”Ć4£¬CµÄĪļÖŹµÄĮæĪŖ y mo
”Ć3”Ć4£¬CµÄĪļÖŹµÄĮæĪŖ y mo l”£
l”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 2A(g) + B(g) =" 2C" (g) ”£Čō¾2sŗó²āµĆCµÄÅضČĪŖ 0.6mol/L £¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
2A(g) + B(g) =" 2C" (g) ”£Čō¾2sŗó²āµĆCµÄÅضČĪŖ 0.6mol/L £¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A£®ÓĆĪļÖŹA±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ0.6mol/£ØL”¤s£© | B£®ÓĆĪļÖŹB±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ0.3mol/£ØL”¤s£© | C£®2sŹ±ĪļÖŹAµÄ×Ŗ»ÆĀŹĪŖ30£„ | D£®2sŹ±ĪļÖŹBµÄÅضČĪŖ0.3mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 qC(g)µÄÕż·“Ó¦ĪŖĪüČČ·“Ó¦£¬m + n < q£¬ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ·“Ó¦“ļµ½Ę½ŗāŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
qC(g)µÄÕż·“Ó¦ĪŖĪüČČ·“Ó¦£¬m + n < q£¬ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ·“Ó¦“ļµ½Ę½ŗāŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ±¶
±¶²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com