
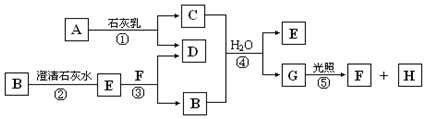
 图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去).
图中A~H均为中学化学中常见的物质,A、B、H是气体,它们之间有如图转化关系(反应中生成的水已略去).分析 A为黄绿色气体,应为Cl2,与石灰乳反应得到C,C能与气体B反应得到E,而E与石灰水反应也得到E,可推知B为CO2,则E为CaCO3,C为Ca(ClO)2,D为CaCl2,G为HClO,F为HCl,H为O2,据此解答;
解答 解:A为黄绿色气体,应为Cl2,与石灰乳反应得到C,C能与气体B反应得到E,而E与石灰水反应也得到E,可推知B为CO2,则E为CaCO3,C为Ca(ClO)2,D为CaCl2,G为HClO,F为HCl,H为O2,
(1)由以上分析可知,E为CaCO3,G为HClO,名称为次氯酸,
故答案为:CaCO3;次氯酸;
(2)C为Ca(ClO)2,C物质在日常生活中可作漂白剂或消毒剂,
故答案为:漂白剂或消毒剂;
(3)反应①的化学方程式为2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O,C为Ca(ClO)2,C与浓盐酸反应,可以生成A气体即氯气,反应的化学方程式为Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O,
故答案为:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O.
点评 本题考查无机物的推断,A的颜色为推断突破口,再结合转化关系推断B为二氧化碳,综合考查元素化合物的性质以及应用,侧重于学生分析能力和综合运用化学知识的考查,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只由一种元素的阳离子与另一种元素的阴离子组成的物质不一定是纯净物 | |
| B. | 用加热的方法可以除去混在NaCl固体中的NH4Cl,说明NH4Cl会升华 | |
| C. | SO2气体和Cl2均能使品红溶液褪色,说明两者均有强氧化性 | |
| D. | 浓硫酸不能用来干燥HI、CO、SO2等气体,因为浓硫酸具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
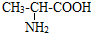 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 药品柜 | 甲 | 乙 | 丙 | 丁 |
| 药品 | 硫黄、红磷 | 镁、锌 | 硫酸、硝酸 | 氢氧化钠、氢氧化钙 |
| A. | 甲柜 | B. | 乙柜 | C. | 丙柜 | D. | 丁柜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
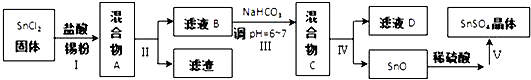
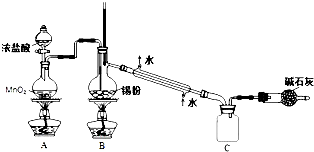
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com