
| A. | XO3- | B. | XO32- | C. | XO42- | D. | XO43- |
科目:高中化学 来源: 题型:选择题
 ,下列叙述正确的有( )
,下列叙述正确的有( )| A. | 分子间可形成氢键 | B. | 分子中既有极性键又有非极性键 | ||
| C. | 分子中有7个σ键和1个π键 | D. | C原子的杂化方式是sp2和sp3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
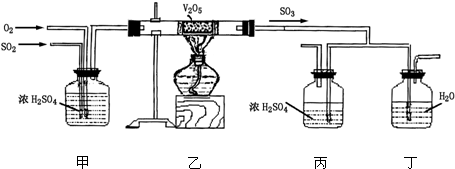
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N元素的电负性较大,但N2的化学性质很稳定 | |
| B. | 稀有气体一般难发生反应 | |
| C. | HF比H2O稳定 | |
| D. | HF、HCl、HBr、HI的稳定性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. |  能与Na2CO3溶液反应生成CO2 能与Na2CO3溶液反应生成CO2 | B. |  与BHT互为同系物 与BHT互为同系物 | ||
| C. | BHT久置于空气中不会被氧化 | D. | 两种方法的反应类型都是加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
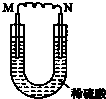
| A. | M上有气体放出 | |
| B. | M为负极,N为正极 | |
| C. | 化学能转变为电能的装置 | |
| D. | 导线中有电流通过,电流方向由N到M |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com