
������ͼ��ˮ�ۺ����õĹ�ҵ����ͼ���ж�����˵����ȷ����
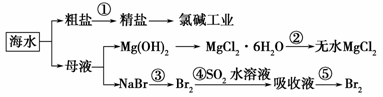
A.��ȥ����������(Mg2+��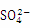 ��Ca2+)�������ҩƷ˳��Ϊ��NaOH��Һ��Na2CO3��Һ��BaCl2��Һ�����˺������
��Ca2+)�������ҩƷ˳��Ϊ��NaOH��Һ��Na2CO3��Һ��BaCl2��Һ�����˺������
B.�ڹ��̢��н�MgCl2·6H2O���ռ����Ƶ���ˮMgCl2
C.������ת���Ƕ��������ȼҵ�еĵ�ⱥ��ʳ��ˮ��һ������ѧ��ת��Ϊ���ܵĹ���
D.�ӵڢ۲����ڢݲ���Ŀ����Ϊ��Ũ��
���𰸡�D
�����������⿼���˺�ˮ��Դ���ۺ����á�A�����̢ټ����ҩƷ˳��ΪBaCl2��Һ��NaOH��Һ��Na2CO3��Һ�����˺�����ᣬ����ٹ��˳���ǰ�������BaCl2��Һ��ϡ����ܳ�ȥ�Ȼ�����Һ�����Ի�������ʣ���A����B���Ȼ�þ��ˮ�⣬Ϊ��ֹˮ�⣬���̢��нᾧ����MgCl2•6H2OҪ�Ȼ����Χ�м�����ˮ�Ƶ���ˮMgCl2����B����C�����ԭ����������ⱥ��ʳ��ˮ�ǵ���ת��Ϊ��ѧ�ܣ���C����D�������ӱ�����Ϊ�嵥�ʺ����������������������ӣ���������������������Ϊ�嵥�ʣ�������Ԫ�أ��ӵڢ۲����ڢݲ���Ŀ����Ϊ��Ũ������D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͬ�¶��£�����3����Ӧ�ų��������ֱ���Q1��Q2��Q3��ʾ����Q1��Q2��Q3�Ĺ�ϵ�ǣ�������
��1��2H2������+O2������═2H2O������+Q1
��2��2H2������+O2������═2H2O��Һ��+Q2
��3��H2������+O2������═H2O������+Q3��
�� A�� Q1��Q2��Q2=2Q3 B�� Q1=Q2=Q3
�� C�� Q1��Q2��Q3=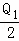 D�� ���Ƚ�
D�� ���Ƚ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶��£���Cl 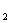 ͨ��NaOH��Һ�У���Ӧ�õ�NaCl��NaClO��NaClO
ͨ��NaOH��Һ�У���Ӧ�õ�NaCl��NaClO��NaClO 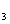 �Ļ��Һ�����ⶨClO - ��ClO
�Ļ��Һ�����ⶨClO - ��ClO 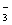 �����Ӹ�����Ϊ1��3����Cl
�����Ӹ�����Ϊ1��3����Cl 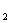 ��NaOH��Ӧʱ����ԭ����ԭ���뱻��������ԭ�ӵĸ�����Ϊ
��NaOH��Ӧʱ����ԭ����ԭ���뱻��������ԭ�ӵĸ�����Ϊ
A.21��5 B.4��1
C.3��1 D.11��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijǿ������ҺX����Ba 2+ ��Al 3+ ��N 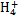 ��Fe 2+ ��Fe 3+ ��C
��Fe 2+ ��Fe 3+ ��C 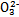 ��S
��S 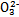 ��S
��S 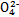 ��Cl - ��N
��Cl - ��N 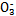 �е�һ�ֻ���,ȡ����Һ����ʵ��,ʵ����������:
�е�һ�ֻ���,ȡ����Һ����ʵ��,ʵ����������:
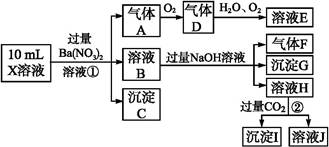
����������Ϣ,�ش���������:
(1)��ҺX�г�H + ��϶����е������� ������ ;����ȷ���Ƿ��е������� ������ ,��Ҫȷ�����������ӵĴ���,��ɿ��Ļ�ѧ������ �������������������� ��
(2)����G�Ļ�ѧʽΪ ������ ��
(3)д���й����ӷ���ʽ:
�����������A ������������������ ��
��������ɳ���I ������������������ ��
(4)����ⶨA��F��I��Ϊ0.01 mol,10 mL X��Һ��n(H + )="0.04" mol,������C���ʵ���0.07 mol,��˵��(1)�в���ȷ���������Ӵ��ڵ������� �������������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1���ܱ������У�����5 mol A���ʣ���һ��������ͬʱ��������������Ӧ��(1)2A(g)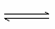 2B(g)��C(g)��(2)A(g)
2B(g)��C(g)��(2)A(g)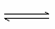 C(g)��D(g)�����ﵽƽ��ʱ�����c(A)=2.5 mol·L��1��c(C)=2.0 mol·L��1��������˵������ȷ����
C(g)��D(g)�����ﵽƽ��ʱ�����c(A)=2.5 mol·L��1��c(C)=2.0 mol·L��1��������˵������ȷ����
| A.�ﵽƽ��ʱA����ת����Ϊ40% | B.�ﵽƽ��ʱc(B)Ϊ1.0 mol·L��1 |
| C.�ﵽƽ��ʱc(B)=2c(D) | D.�ﵽƽ��ʱc(D)Ϊ0.5 mol·L��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й���168O��������ȷ���ǣ�������
�� A�� ������Ϊ8 B�� ������Ϊ8 C�� ������Ϊ16 D�� ������Ϊ16
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��״���µ�1molH2�����ԼΪ��������
�� A�� 11.2 L B�� 22.4 L C�� 33.6 L D�� 44.8 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ij������Ʒ����ʯ�һ�ϣ����ŵ���ζ��������û�����Ʒ�к��У�������
�� A�� K+ B�� NO3﹣ C�� NH4+ D�� SO42﹣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
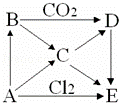
A��E�������ʼ���ת����ϵ��ͼ��ʾ������AΪ���ʣ�BΪ����ɫ�Ĺ��壮���ƶϣ����û�ѧʽ��ʾ��
A������B��������C�ǣ�D��������E��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com