
【题目】标准状况下,![]() 某无色可燃性气体在足量氧气中完全燃烧。将产物通入足量澄清石灰水中,得到白色沉淀的质量为
某无色可燃性气体在足量氧气中完全燃烧。将产物通入足量澄清石灰水中,得到白色沉淀的质量为![]() ;若用足量碱石灰吸收燃烧产物,则碱石灰增重
;若用足量碱石灰吸收燃烧产物,则碱石灰增重![]() 。
。
(1)计算燃烧产物中水的质量_____________。
(2)若原气体是单一气体,通过计算推断它的分子式___________________。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式________________(只要求写出一组)。
【答案】![]()
![]()
![]() 、
、![]() (或
(或![]() 、
、![]() 或
或![]() 、
、![]() )
)
【解析】
(1)气体燃烧生成CO2的质量为![]() ;碱石灰增重为二氧化碳和水的质量之和,所以气体燃烧生成H2O的质量为9.3g-6.6g=2.7g;
;碱石灰增重为二氧化碳和水的质量之和,所以气体燃烧生成H2O的质量为9.3g-6.6g=2.7g;
(2)标准状况下,1.68L气体的物质的量为![]() ;所以1mol该气体中含碳的物质的量为
;所以1mol该气体中含碳的物质的量为![]() ,含氢的物质的量为
,含氢的物质的量为![]() 4.0mol;又因该物质在标准状况下为气体,故其一定不含有氧元素,则该气体的分子式为
4.0mol;又因该物质在标准状况下为气体,故其一定不含有氧元素,则该气体的分子式为![]() ;
;
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,则在2mol混合气体中,应含有4molC原子、8molH原子,故这两种气体可以是C4H6和H2按1:1组成的混合气体,也可以是C3H8与CO或C3H6与CH2O按1:1组成的混合气体。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】某学生用标准0.1400molL-1NaOH溶液滴定未知浓度硫酸的实验操作如下。
A.用酸式滴定管取稀H2SO425.00mL,注入锥形瓶中,加入酚酞。
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2-3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度,用去NaOH溶液15.00mL。
(1)①滴定操作的正确顺序是(用序号填写)___;②在G操作中如何确定终点?___。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”)___。
(3)配制100mLNaOH标准溶液,必须使用到的玻璃仪器是___。
(4)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值___(选填“偏大”“偏小”或“无影响”)
(5)计算待测硫酸溶液的物质的量浓度___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,用蒸馏水稀释1 mol/L氨水至0.01 mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
A.![]() B.c(H+)·c(OH-)
B.c(H+)·c(OH-)
C.![]() D.c(OH-)
D.c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镓有“电子工业脊梁”的美誉,它与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图所示:

(1)元素Ga位于Al的下一周期,写出镓(Ga)的原子结构示意图为____________CO2的电子式为_____________________
(2)下列有关Al、Ga的说法不正确的是______
A.由流程图可知酸性:Al(OH)3>Ga(OH)3 B.Ga2O3可与盐酸反应生成GaCl3
C.Ga(OH)3可由Ga2O3与水反应得到 D.与酸反应的剧烈程度:Al<Ga
(3)图中涉及到的Al、Na、O三种元素简单离子半径由大到小的顺序_____________
(4)步骤二中不能通入过量的CO2,理由_________________(用离子方程式表示)
(5)工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含Zn、Fe、Cu杂质,以NaOH水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:Zn2+<Ga3+<Fe2+)
①下列有关电解精炼说法正确的是_______
A.阳极发生氧化反应,其主要电极反应式:Ga-3e- ═ Ga3+
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.在阴极除了析出高纯度的镓之外,还有H2产生
D.电解后,电解槽底部的阳极泥中只有Cu和Fe
②阴极析出高纯度镓的电极反应式__________________________________
(6)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。氮化镓(GaN)的一种制备方法是采用GaCl3与NH3在一定条件下反应,写出该反应的化学方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以![]() 、
、![]() 、
、![]() 、
、![]() 的形式存在。
的形式存在。

回答下列问题:
![]() 中Zn的化合价为_______,“溶浸”中ZnO发生反应的离子方程式为_______。
中Zn的化合价为_______,“溶浸”中ZnO发生反应的离子方程式为_______。
![]() 锌浸出率与温度的关系如图所示,分析
锌浸出率与温度的关系如图所示,分析![]() 时锌浸出率最高的原因为_______。
时锌浸出率最高的原因为_______。

![]() “氧化除杂”中,
“氧化除杂”中,![]() 转化为
转化为![]() 胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为_______。
胶体吸附聚沉除去,溶液始终接近中性。该反应的离子方程式为_______。
![]() “滤渣3”的主要成分为_______。
“滤渣3”的主要成分为_______。
![]() “电解”时
“电解”时![]() 在阴极放电的电极反应式为______。阳极区放出一种无色无味的气体,将其通入滴有KSCN的
在阴极放电的电极反应式为______。阳极区放出一种无色无味的气体,将其通入滴有KSCN的![]() 溶液中,无明显现象,该气体是_______
溶液中,无明显现象,该气体是_______![]() 写化学式
写化学式![]() 。电解后的电解液经补充_______
。电解后的电解液经补充_______![]() 写一种物质的化学式
写一种物质的化学式![]() 后可返回“溶浸”工序继续使用。
后可返回“溶浸”工序继续使用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电子排布式或轨道表示式正确的是( )
①C原子的轨道表示式:![]()
②Cr原子的电子排布式:1s22s22p63s23p63d44s2
③O原子的轨道表示式:![]()
④Br原子的外层电子排布式:3d104s24p5
⑤B原子的轨道表示式:![]()
A.① ② ③B.② ③ ④C.① ② ④ ⑤D.只有③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到检流计的指针发生了偏转。
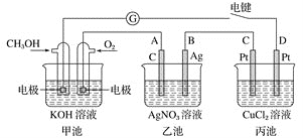
请回答下列问题:
(1)甲池为________(填“原电池”、“电解池”或“电镀池”),通入CH3OH一极的电极反应式为_____________________________________________________________;
(2)乙池中A(石墨)电极的名称为________(填“正极”、“负极”、“阴极”或“阳极”),总反应式为_________________________________________________________;
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗O2的体积为________ mL(标准状况),丙池中________极析出________ g铜;
(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将________(填“增大”、“减小”或“不变”);丙中溶液的pH将________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼![]() 又称联氨,是一种可燃性的液体,可用作火箭燃料。
又称联氨,是一种可燃性的液体,可用作火箭燃料。
![]() 已知在101kPa时,
已知在101kPa时,![]() 时,
时,![]() 在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则
在氧气中完全燃烧生成氮气和水,放出624kJ的热量,则![]() 的燃烧热的热化学方程式是_____________。
的燃烧热的热化学方程式是_____________。
![]() 下图是一个电化学过程示意图。
下图是一个电化学过程示意图。

![]() 图中甲池是_________
图中甲池是_________![]() 填“原电池”或“电解池”
填“原电池”或“电解池”![]() ,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
,其电解质溶液为KOH溶液,则该池电极M的电极反应式是_________________________。
![]() 乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成
乙池中石墨电极2的电极反应式是_________________________。 当石墨电极2上生成![]() 气体时
气体时![]() 标准状况下
标准状况下![]() ,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________
,转移的电子的数目为_________,则甲池理论上消耗标标准状况下的空气是________![]() 假设空气中氧气体积含量为
假设空气中氧气体积含量为![]() 。
。
![]() 传统制备肼的方法,是以NaClO氧化
传统制备肼的方法,是以NaClO氧化![]() ,制得肼的稀溶液。该反应的离子方程式是_________。
,制得肼的稀溶液。该反应的离子方程式是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com