
 2015��8��12�Žӽ���ҹʱ�֣�����������һ����װ����ͷ������ը��������ը���Ǽ�װ���ڵ���ȼ�ױ���Ʒ����ը������죬��������Ģ���ƣ��������յ���Ϣ������װ������Σ�ջ�ѧƷ�����мء��ơ������ơ�����ء��ռ��軯�ơ�������ϩ���ȵ���ȣ��˵�����Σ�ջ�ѧƷ�����л����������������ᡢ����李��軯�ơ�4��6-��������-���ٶ������ӵȣ�
2015��8��12�Žӽ���ҹʱ�֣�����������һ����װ����ͷ������ը��������ը���Ǽ�װ���ڵ���ȼ�ױ���Ʒ����ը������죬��������Ģ���ƣ��������յ���Ϣ������װ������Σ�ջ�ѧƷ�����мء��ơ������ơ�����ء��ռ��軯�ơ�������ϩ���ȵ���ȣ��˵�����Σ�ջ�ѧƷ�����л����������������ᡢ����李��軯�ơ�4��6-��������-���ٶ������ӵȣ����� ��1��ͬ����Ԫ�ص�һ������������ҳ��������ƣ�ͬ�������϶���Ԫ�ص�һ��������С����Nԭ�ӵ�2p�ܼ�Ϊ�����ȶ�״̬����һ�����ܸ���ͬ��������Ԫ�صģ�
��2����ˮ�����γ�������������ʵ��ܽ�ȣ��ռ��������Ӻ����������ɣ��������Ӿ��壻S2-���Ӻ��������Ϊ18�������������ԭ������д���̬�����Ų�ʽ��
��3��NO3-�����е�ԭ�ӵŵ��Ӷ���=$\frac{5+1-2��3}{2}$=0���۲���Ӷ���=3+0=3��
��4��ԭ��������ȡ��۵�������Ҳ��ȵ�����Ϊ���ӣ�CN-��N2��Ϊ�ȵ����壬CN-�к���C��N�����������к���1���Ҽ���2���м�����������ȡ�����ķ�Ӧ��֪���軯�ơ��������̺�Ũ�����ڼ����������Ƶã�CN��2�������������̡���������ˮ��
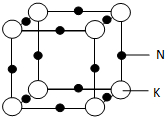
��5�����ݾ�̯�����㾧����Na��Kԭ����Ŀ��ȷ���Ͻ�Ļ�ѧʽ�����ݾ���ͼ��֪��ÿ��K ԭ����Χ��6����ԭ�ӣ����ݾ����Ľṹ��֪�������ı߳�Ϊ��ԭ�Ӻͼ�ԭ�ӵ�ֱ��֮�ͣ�����Ŀռ�������Ϊ$\frac{������Na��Kԭ�������}{�������}$��100%��
��� �⣺��1��ͬ����Ԫ�ص�һ������������ҳ��������ƣ�ͬ�������϶���Ԫ�ص�һ��������С����Nԭ�ӵ�2p�ܼ�Ϊ�����ȶ�״̬����һ�����ܸ�����Ԫ�صģ���NH4NO3��NaCN�������ʵ�Ԫ���е�һ������������N��
�ʴ�Ϊ��N��ͬ����Ԫ�ص�һ������������ҳ��������ƣ�ͬ�������϶���Ԫ�ص�һ��������С����Nԭ�ӵ�2p�ܼ�Ϊ�����ȶ�״̬����һ�����ܸ�����Ԫ�صģ�
��2��������ˮ�γ�����������������ܣ��ʶ�������ͼ������ܽ�Ƚϴ���Ǽ��ᣬ�ռ��������Ӻ����������ɣ������ռ������Ӿ��壬S2-���Ӻ�����18�����ӣ����̬�����Ų�ʽΪ1s2s22p63s23p6��
�ʴ�Ϊ�����������ˮ�γ���������Ӿ��壻1s2s22p63s23p6��
��3��NO3-�����е�ԭ�ӵŵ��Ӷ����T$\frac{5+1-2��3}{2}$=0���۲���Ӷ���=3+0=3������NO3-���幹��Ϊƽ�������Σ�����ԭ�ӵ�ԭ�ӵ��ӻ��������sp2��
�ʴ�Ϊ��ƽ�������Σ�sp2��
��4��ԭ��������ȡ��۵�������Ҳ��ȵ�����Ϊ���ӣ�CN-��N2��Ϊ�ȵ����壬���߽ṹ���ƣ�CN-�к���C��N�����������к���1���Ҽ���2���м���������1mol������NaCN��CN-�����Ħм���Ϊ2NA��CN-�к�������ԭ�ӡ�10���۵��ӣ���CN-��Ϊ�ȵ�����ķ�����CO��N2��
������ȡ�����ķ�Ӧ��֪���軯�ơ��������̺�Ũ�����ڼ����������Ƶã�CN��2����Ӧ��ѧ����ʽΪ��2NaCN+MnO2+2H2SO4$\frac{\underline{\;\;��\;\;}}{\;}$��CN��2+Na2SO4+MnSO4+2H2O��
�ʴ�Ϊ��2NA��CO��N2��2NaCN+MnO2+2H2SO4$\frac{\underline{\;\;��\;\;}}{\;}$��CN��2+Na2SO4+MnSO4+2H2O��
��5�������У���ԭ����Ϊ12��$\frac{1}{4}$=3����ԭ����Ϊ8��$\frac{1}{8}$=1�����ԺϽ�Ļ�ѧʽΪKNa3��
���ݾ���ͼ��֪��ÿ��K ԭ����Χ��6����ԭ�ӣ����Ծ�����K ԭ�ӵ���λ��Ϊ6��
��������ԭ�Ӻͼ�ԭ�����֮��Ϊ$\frac{4}{3}$��[��186pm��3��3+��227pm��3]�������ı߳�Ϊ��ԭ�Ӻͼ�ԭ�ӵ�ֱ��֮��Ϊ2����186pm+227pm�������Ծ��������Ϊ��2��186pm+2��227pm��3������Ŀռ�������Ϊ$\frac{4}{3}$��[��186pm��3��3+��227pm��3]�£�2��186pm+2��227pm��3}��100%=$\frac{\frac{4}{3}�У�186{\;}^{3}��3+227{\;}^{3}��}{��186��2+227��2��^{3}}$��100%��
�ʴ�Ϊ��KNa3��6��$\frac{\frac{4}{3}�У�186{\;}^{3}��3+227{\;}^{3}��}{��186��2+227��2��^{3}}$��100%��
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰�����ܡ���������Ų����ӻ���ʽ��ռ乹�͡��ȵ����塢��������ȣ��Ѷ��еȣ�������ѧ���ķ��������ͼ��������Ŀ��飬ע�����֪ʶ���������գ�


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ȼ��������ĸ��������Һ��Ȼ���ټ���ˮ | |
| B�� | ����Ũ�����Ũ������ټ��� | |
| C�� | �ȼ�����������ˮ��Ȼ���ټ���������������Һ | |
| D�� | ��ȼ����Һ�壬Ȼ���ٹ۲����������̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�� | ���������� | ���� |
| A | ����װ�������ԣ� | ��ע���������������һ�ξ�������֣��ܹ��ָ�ԭλ | ���������� |
| B | 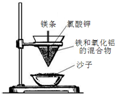 | ��ȼþ�������䣬���������в������ȵĽ��� | ���ȷ�Ӧ�� 2Fe+Al2O3$\frac{\underline{\;����\;}}{\;}$2Al+Fe2O3 |
| C | ��SO2����ͨ����������Һ�� | �л�ɫ���Dz��� | ��ԭ�ԣ�H2S��SO2 |
| D | �Ʊ�CuSO4 | ����һ����Cu��Ũ���ᷴӦ ����������Cu��ϡ�����ڲ���ͨ��O2������·�Ӧ | ��������������ɫ��ѧ���� ����һ��ԭ�������ʸ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
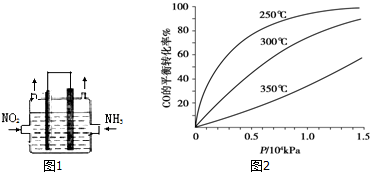
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ϊ�ӳ�ʳƷ�����ڣ��������д������ӱ������Ƶȷ����� | |
| B�� | ��ת��������β��Ϊ�����壬����������������ķ��� | |
| C�� | PM2.5��ָ�����е���������������ﺬ��֮�� | |
| D�� | ����Ƥ������Ϊԭ�������ֽ������Ҫ�ɷ�����ά�أ�����ά������۲���ͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
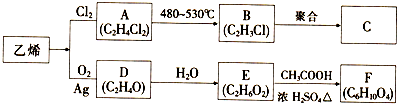
 ��
��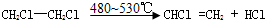 ��
��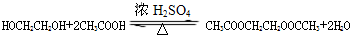 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��Z�Ļ�ѧʽΪSiO2��
��Z�Ļ�ѧʽΪSiO2���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com