
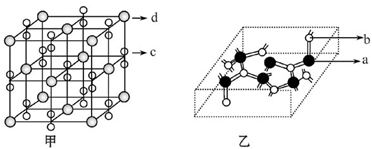
 3d104s1
3d104s1 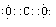 ;基态f原子的外围电子的排布式为3d104s1 ;
;基态f原子的外围电子的排布式为3d104s1 ;

科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Br>Se>Cl | B.热稳定性:HCl>H2Se>HBr |
| C.酸性:H2SeO4>HBrO4>HClO4 | D.还原性:Se2—>Br—>Cl— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
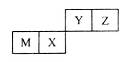
| A.Y元素气态氢化物的稳定性大于Z元素的 |
| B.M和Y两种元素,可以形成电子层结构相同的两种简单离子 |
| C.X元素最高价氧化物对应水化物的酸性弱于Y元素的 |
| D.M元素的氧化物既可以与酸溶液反应,也可以与碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10Be和9Be是中子数不同质子数相同的不同原子 |
| B.10Be的原子核内中子数比质子数多 |
| C.5.2 g26Al3+中所含的电子数约为1.2×1024 |
| D.26Al和26Mg的质子数、中子数和核外电子数都不相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性:H2SO4>HClO4>HBrO4 | B.碱性:NaOH>KOH>RbOH |
| C.非金属性: P>S>Cl | D.气态氢化物稳定性:HF>H2O>PH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B.若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C.若M属于离子化合物,则该化合物中只存在离子键 |
| D.若M属于离子化台物,则该化合物中原子个数比可能为1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Y、Z、X、W的原子序数依次减小 |
| B.X的简单氢化物的沸点低于Y的简单氢化物的沸点 |
| C.由W、X、Y、Z四种元素组成的化合物可能显强酸性 |
| D.W和X形成的化合物,与W和Y形成的化合物中各元素质量比可能相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子序数是24 |
| B.元素周期表中硒位于第四周期第VIA族 |
| C.最高价氧化物是SeO3,是酸性氧化物 |
| D.气态氢化物化学式是H2Se,稳定性比HCl差 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.随原子序数的递增,元素原子的核外电子数增多,原子半径逐渐减小 |
| B.若两种不同的核素具有相同的中子数,则二者一定不属于同种元素 |
| C.在化学反应中,原子首先失去的电子能量最低 |
| D.在元素周期表中,各主族元素的最高化合价与其族序数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com