
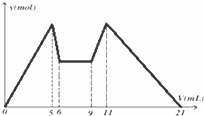
如图是向MgCl2、AlCl3混合溶液中,先后加入试剂A、B时所得沉淀物质的量y(mol) 与试剂体积V(mL)间的关系图.开始滴加6mL试剂A后继续滴加A若干,之后改滴试剂B.以下结论正确的是( )
|
| A. | 可能是NaOH,B可能是盐酸,且2C(A)=C(B) |
|
| B. | 若A和B均为一元强酸或一元强碱,则滴加7mL试剂A后改滴试剂B |
|
| C. | A可能是Ba(OH)2,B可能是硫酸,且C(A)=C(B) |
|
| D. | 原混合液中,c(Al3+):c(Mg2+):c(Cl﹣)=1:2:7 |
| 有关混合物反应的计算;镁、铝的重要化合物. | |
| 分析: | A、氯化镁和氯化铝与盐酸不反应,氢氧化钠和氯化镁、氯化铝反应,结合图片分析确定正误; B、根据沉淀的量未发生变化确定反应实质,从而确定所加试剂的变化情况; C、根据铝元素守恒计算酸和碱浓度的关系; D、根据第一次沉淀最大到最小需要的氢氧化钠的量计算铝离子的物质的量,根据需要氢氧化钠总的物质的量计算镁离子的物质的量,根据电荷守恒计算氯离子的物质的量. |
| 解答: | 解:A、根据加入前6mL试剂时,先有沉淀生成而后溶解,所以试剂A是NaOH,则B可能是盐酸,氢氧化铝转化为偏铝酸钠消耗的氢氧化钠的体积是偏铝酸钠转化为氢氧化铝消耗的盐酸体积的一半,所以氢氧化钠浓度是盐酸的浓度的2倍,cA=2cB,故A错误; B、若A和B均为一元强酸或一元强碱,根据二者的浓度比 c(A)=2c(B),则滴加7mL试剂A后改滴试剂B,故B正确; C、如果A是Ba(OH)2,B是硫酸,则会发生反应生成硫酸钡,硫酸钡不溶于过量的酸中,沉淀最终的量不是零,故C错误; B、从加入5 mL A生成沉淀最多,再继续加1 mL A沉淀量减少到最小值,相应反应的离子方程式为Al(OH)3+OH﹣=AlO2﹣+2H2O,由此可知,n(Al3+)=n〔Al(OH)3〕=(1×6×10﹣3) mol;由前5 mL NaOH形成最大沉淀量可知,2n(Mg2+)+3n(Al3+)=(5×10﹣3×6)mol,所以n(Mg2+)=(1×6×10﹣3) mol,由溶液中阴阳离子所带电荷相等得n(Cl﹣)=(5×10﹣3×6)mol,即溶液中c(Mg2+):c(Al3+):c(Cl﹣)=1:1:5,故D错误. 故选:B. |
| 点评: | 本题考查了镁、铝重要化合物的性质,难度较大,能正确分析图象中转折线发生的化学反应是解本题的关键. |


科目:高中化学 来源: 题型:
下列条件能发生消去反应的是( )
A.溴乙烷与NaOH醇溶液共热
B.一氯甲烷与NaOH醇溶液共热
C. 溴乙烷与NaOH水溶液共热
溴乙烷与NaOH水溶液共热
D.乙醇与浓硫酸共热至170 ℃
查看答案和解析>>
科目:高中化学 来源: 题型:
在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征反应对物质进行区别、检验等。下列说法正确的是
A.用KOH溶液可以将NH4Cl、NaBr、CuSO4、FeCl3区别开
B.C、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸不能将它们区别开
C.某溶液中加入稀盐酸有无色气体产生,该气体能使澄清石灰水变浑浊,则此溶液中一定含有CO32¯
D.可以用BaCl2溶液和稀硝酸检验Na2SO3是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液既能溶解Al(OH)3,又能溶解Al,但不能溶解Fe,在该溶液中可以大量共存的离子组是( )
|
| A. | K+、Na+、HCO | B. | Na+、SO |
|
| C. | NH | D. | H+、K+、Cl﹣、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
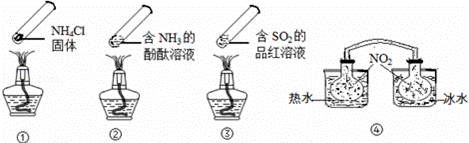
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
|
| A. | 加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好 |
|
| B. | 加热时,②、③溶液均变红,冷却后又都变为无色 |
|
| C. | ④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅 |
|
| D. | 四个“封管实验”中所发生的化学反应都是可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某强碱性溶液中可能含有K+、NH4+、Al3+、AlO2﹣、SO42﹣、SiO32﹣、CO32﹣、Cl﹣中的某几种离子,现进行如下实验:
①取少量溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成.
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
(1)原溶液中肯定存在的离子是 肯定不存在的离子是
(2)已知一定量的原溶液中慢慢滴入5mL 0.2mol/L盐酸时,产生的沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl﹣?(通过列式说明) .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关利用乙醛制备银镜过程的说法不正确的是
A.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水至最初的沉淀恰好溶解为止
B.将几滴银氨溶液滴入2 mL乙醛中
C.将盛有乙醛与银氨溶液混合液的试管置于热水浴中加热
D.在银氨溶液的配制过程中溶液pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
根据要求完成下列实验。(a、b 为弹簧夹,其他装置略去)
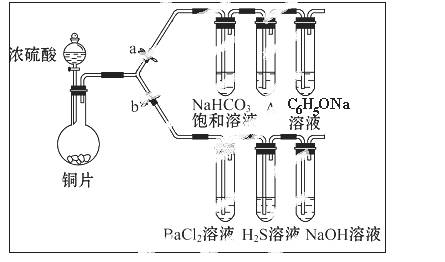
(一)验证酸性的相对强弱:碳酸>苯酚。(已知酸性:亚硫酸 >碳酸)
(1)铜与浓硫酸反应的化学方程式是_________________________________________,
装置A中的足量的试剂是 。
(2)连接仪器、 、加药品后,打开a关闭 b,然后滴入浓硫酸,加热。能说明碳酸的酸性比苯酚酸性强的实验现象是:____________________________。
(二)验证SO2具有氧化性、还原性和酸性氧化物的通性。
(3)打开b,关闭a。能验证SO2具有氧化性的化学方程式是_______________________。
(4)若过量的SO2通入NaOH溶液中,其化学方程式是:____________________________。
(5)BaCl2溶液中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀化学式分别是__________________,_________________。
(6)写出其中SO2 显示还原性并生成白色沉淀的总的离子方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能 含有K+、
含有K+、
Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO 、SO
、SO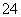 、Cl-中的若干种离子,该小组同学取100 mL水样进
、Cl-中的若干种离子,该小组同学取100 mL水样进
行实验:向样品中先滴加硝酸钡溶液,再滴加1 mol·L-1硝酸,实验过程中沉淀质量的变化如图所示:
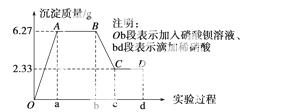
(1)水样中一定含有的阴离子是____________,其物 质的量浓度之比为________。
质的量浓度之比为________。
(2)写出BC段曲线所表示反应的离子方程式:______________________________。
(3)由B点到C点变化过程中消耗硝酸的 体积为_
体积为_ _______。
_______。
(4)试根据实验结果推测K+是否存在?____(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是________________(若K+不存在,则不必回答)。
(5)设计简单实验验证原水样中可能存在的离子:
________________________________________ _______________________________
_______________________________
________________________________________________________________________
________________________________________________________________________。(写出实验步骤、现象和结论)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com