
| A、足量的硫单质与64g铜反应,有2mol电子发生转移 |
| B、常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,Kap(AgCl)增大 |
| C、0.1mol?L-1Na2CO3中加入少量NaOH固体振荡,c(Na+)和c(CO32-)都增大 |
| D、相同浓度的CH2COOH和CH2COONa溶液等体积混合后,则:c(CH2COO-)+c(CH2COOH)=c(Na+) |


科目:高中化学 来源: 题型:
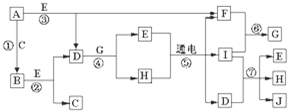
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、纯铝制品在空气中表面逐渐失去金属光泽 |
| C、锌与稀硫酸反应时,往溶液中滴入几滴CuSO4溶液可以使反应变快 |
| D、与电源的负极相连的金属不易生锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O3+2KI+H2O═2KOH+I2+O2 | ||||
| B、3NO2+H2O═2HNO3+NO | ||||
| C、3S+6NaOH═Na2SO3+2Na2S+3H2O | ||||
D、4HCl(浓)+MnO2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0LPH=1的H2SO4溶液中所含H+数为0.2 NA |
B、26g (聚乙炔)所含碳碳双键数为2 NA (聚乙炔)所含碳碳双键数为2 NA |
| C、1moAl13-团簇离子的最外层电子总数为40 NA |
| D、标准状况下,22.4LCO、CO2混合气体中所含碳原子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaH是离子化合物,则NaH的电子式为Na:H |
| B、碘-131是一种放射性元素,其简单阴离子的核外电子数为53 |
| C、等物质的量的HCl和NaCl中分子数相等 |
| D、核素A与核素B的质量数相等,中子数不相等,它们一定不是同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com