
【题目】黑火药爆炸时发生化学反应:S+2KNO3+3C→K2S+3CO2↑+N2↑,完成下列填空:
(1)上述反应涉及的元素中,非金属性最强的是___,试写出属于第二周期的元素的原子半径大小有___>___>___。(填元素符号)
(2)上述反应的生成物中,属于离子化合物的是___,其电子式为___。
(3)硫元素的气态氢化物所含化学键类型为___(填“离子键”或“共价键”),其水溶液长期遭空气中放置容易变浑浊,用化学方程式表示该变化___,该变化体现出硫元素的非金属性比氧元素___(填“强”或“弱”)。
【答案】O C N O K2S ![]() 共价键 2H2S+O2=2H2O+S↓ 弱
共价键 2H2S+O2=2H2O+S↓ 弱
【解析】
(1)该反应中的非金属元素为C、N、O、S,同周期从左向右,原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强;同主族从上到下,原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱;
(2)由离子键构成的化合物为离子化合物;
(3)硫元素的气态氢化物为H2S,属于共价化合物,其水溶液长期遭空气中放置,H2S可与空气中的O2发生反应;
(1)C、N、O位于同周期,从左向右,半径逐渐减小,因此半径C> N >O,非金属性逐渐增强,即O> N > C, O和S位于同主族,半径逐渐增大,因此半径S>O非金属性逐渐减弱,因此O>S,综上,非金属性最强的是O,第二周期的元素原子半径C> N >O;
(2)反应的生成物中由离子键构成的化合物为K2S,电子式为:![]() ;
;
(3)硫元素的气态氢化物为H2S,属于共价化合物,含有共价键;H2S的水溶液长期遭空气中放置,其中的H2S可与空气中的O2发生反应,方程式为:2H2S+O2=2H2O+S↓,反应中O2能置换出S单质,说明硫元素的非金属性比氧元素弱。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)主要用作棉纺、造纸业的漂白剂,也可用于食品消毒、水处理等,亚氯酸钠受热易分解。以氯酸钠(NaClO3)等为原料制备亚氯酸钠的工艺流程如下:

(1)ClO2中Cl的化合价为________。
(2)从“母液”中回收的主要物质是________(填化学式)。
(3)“冷却结晶”后需________(填操作名称),该操作用到的玻璃仪器有________。
(4)反应2中转移0.1NA个电子时,生成NaClO2的质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以某硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如下:

下列说法不正确的是
A. “酸溶”中加热或搅拌或适当增大硫酸浓度均可加快溶解速度
B. 滤渣的主要成分是SiO2和Fe
C. “沉铁”过程中生成Fe(OH)2的化学方程式为: FeSO4+2NH4HCO3===Fe(OH)2↓+ (NH4)2SO4+ 2CO2↑。
D. “氧化”Fe(OH)2浆液时,可用氯气代替空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、X、Y六种物质均由短周期元素组成,其中X为常见离子化合物,它们之间的转换关系如下图所示

(1)已知条件I和条件II相同,则该反应条件为____________________ 。
(2)物质X的电子式为_____________________ 。
(3)写出B与Ca(OH)2反应的化学方程式______________________________ 。
(4)写出X在条件II下反应生成B、C、D的离子方程式_____________________________________________ 。
(5)写出实验室制B的化学方程式,并标出电子转移方向、数目____________________________________________ 。
(6)请简述鉴定物质X的实验方法____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盐酸和氯化铝的混合液中不断滴加氢氧化钠溶液,下列图象中,能正确表示上述反应的是(横坐标表示加入氢氧化钠溶液的体积,纵坐标表示反应生成沉淀的质量)( )
A. B.
B.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一容积可变的容器中,反应2A(g)+B(g)![]() 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是( )
A.均减半B.均加倍C.均增加1molD.均减少1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组以废弃的易拉罐、漂白粉、氢氧化钠等为原料制造了一种新型环保电池,并进行相关实验,如图所示。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO![]() +H2O。下列说法正确的是
+H2O。下列说法正确的是
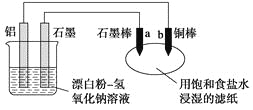
A. 电池的负极反应式为:ClO-+H2O+2e-=Cl-+2OH-
B. 当有0.1 mol Al完全溶解时,流经电解液的电子数为1.806×1023个
C. 往滤纸上滴加酚酞试液,b极附近颜色变红
D. b极附近会生成蓝色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“太阳水”电池装置如图所示,该电池由三个电极组成,其中a为TiO2电极,b为Pt电极,c为WO3电极,电解质溶液为pH=3的Li2SO4-H2SO4溶液。锂离子交换膜将电池分为A、B两个区,A区与大 气相通,B区为封闭体系并有N2保护。下列关于该电池的说法错误的是( )
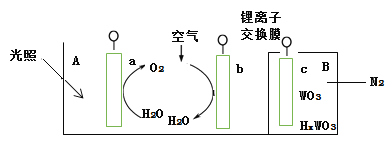
A.若用导线连接a、c,则a为负极,该电极附近pH减小
B.若用导线连接a、c,则c电极的电极反应式为HxWO3 - xe- =WO3 + xH+
C.若用导线先连接a、c,再连接b、c,可实现太阳能向电能转化
D.若用导线连接b、c, b电极的电极反应式为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋占据地球面积的![]() ,拥有丰富的资源,从海洋中可以提取钠、镁、溴、碘等物质。提取溴的过程有一步反应的离子方程式:
,拥有丰富的资源,从海洋中可以提取钠、镁、溴、碘等物质。提取溴的过程有一步反应的离子方程式:![]() 。下列叙述错误的是
。下列叙述错误的是
A.![]() 为还原剂B.
为还原剂B.![]() 既不是氧化剂,又不是还原剂
既不是氧化剂,又不是还原剂
C.生成![]() ,转移
,转移![]() 电子D.
电子D.![]() 仅为氧化产物
仅为氧化产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com