
下表是部分短周期元素的原子半径及主要化合价,根据表中的信息,判断下面叙述正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径(nm) | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
科目:高中化学 来源: 题型:单选题
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成1HmX分子,在a g 1HmX中所含质子的物质的量是
A.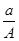 (A-N+m)mol (A-N+m)mol | B.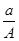 (A-N)mol (A-N)mol |
C.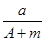 (A-N)mol (A-N)mol | D.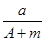 (A-N+m)mol (A-N+m)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列比较或归纳正确的是( )
| A.稳定性:NH3<PH3<ASH3 |
| B.离子半径:Cl->S2->Al3+ |
| C.酸性:HClO4>H2SO4>H3PO4 |
| D.碱性:Be(OH)2>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中错误的是 ( )
| A.原子半径Cl>S>O | B.还原性Na>Mg>Al |
| C.稳定性HF>HCl>HBr | D.酸性HClO4>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
今年5月7日某公司丢失铱-192放射源的事件再次敲响核安全的警钟。下列关于铱-192 (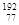 Ir)的说法正确的是
Ir)的说法正确的是
| A.原子序数为77 | B.电子数为115 | C.中子数为192 | D.质量数为77 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D、E五种元素原子序数依次增大,且均不超过18。其中A与C、B与E分别为同族元素。原子半径A<B<E<D<C,B原子最外层电子数是内层电子数的3倍,C、D的核外电子数之和与B、E核外电子数之和相等。下列说法正确的是
A.原子最外层电子数:B<A B.A与E形成的化合物是离子化合物
C.最高价氧化物对应的水化物碱性:C<D D.B与E可以形成EB2型化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com