
【题目】下列说法正确的是 ( )
A. SO2的摩尔质量为64 g
B. 气体的摩尔体积约为22.4 L·mol-1
C. 0.012kg 12C中所含有的碳原子数即为阿伏加德罗常数
D. 4 g NaOH溶于1 L水所得溶液的物质的量浓度为0.1 mol·L-1
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】已知甲醛(HCHO)分子中的4个原子共处于同一平面上.下列分子中所有原子不可能同时共存于同一平面上的是( )
A.苯乙烯 ![]()
B.苯甲醛 ![]()
C.苯乙酮 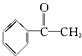
D.苯酚 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.萃取振荡操作时,要及时打开分液漏斗放气
B.分液漏斗和容量瓶在使用前都要检漏;可以用酒精代替CCl4萃取碘水中的碘单质
C.蒸馏时加入沸石的目的是为了防止暴沸;蒸馏时温度计水银球应插入烧瓶内液面下
D.粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是表示铁原子和铁离子的3种不同化学用语。
结构示意图 | 电子排布式 | 电子排布图 | |
铁 原 子 |
| 1s22s22p63s23p63d64s2 |
|
铁 离 子 |
| 1s22s22p63s23p63d5 |
|
(1)铁原子最外层电子数为 ,铁在发生化学反应时,参加反应的电子可能是 。
(2)请你通过比较、归纳,分别说出3种不同化学用语所能反映的粒子结构信息。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分弱酸的电离平衡常数如表所示.下列反应的离子方程式书写错误的是( )
弱酸 | H2SO3 | HClO | H2CO3 |
Ka1 | 1.54×10﹣2 | 2.95×10﹣8 | 4.30×10﹣7 |
Ka2 | 1.02×10﹣7 | ﹣ | 5.61×10﹣11 |
A.NaClO溶液中通入少量CO2:ClO﹣+H2O+CO2═HCO ![]() +HClO
+HClO
B.氯水中加入少量NaCO3粉末:HCO ![]() +H+═H2O+CO2↑
+H+═H2O+CO2↑
C.NaClO溶液中通入少量SO2:2ClO﹣+H2O+SO2═SO ![]() +2HClO
+2HClO
D.Na2CO2溶液中缓慢通入少量SO2:2CO ![]() +H2O+SO2═SO
+H2O+SO2═SO ![]() +2HCO
+2HCO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验表明;纯硫酸液体的电离能力强于纯硝酸;纯硫酸的导电性强于纯水;又知液态电解质都能像水一样自身电离;而建立电离平衡(即像2H2O![]() H3O++OH-);且在一定温度下都有各自的离子积常数。
H3O++OH-);且在一定温度下都有各自的离子积常数。
据此回答下列问题:
(1)纯硫酸在液态时;自身电离的电离反应方程式是 ;它在25 ℃时的离子积常数K(H2SO4)比水的离子积常数K(H2O) (填“大”“小”或“相等”)。
(2)在纯硫酸与纯硝酸的液态混合物中;存在的阴离子主要是 ;这是因为混合液中不但存在两种电离平衡(即H2SO4和HNO3各自的电离平衡;且硫酸的酸性强于硝酸);又在无水的条件下;混合酸中发生 (写离子反应方程式)反应而造成的。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是( )
A.![]() Cl2与
Cl2与 ![]() Cl2氧化能力相近,二者互为同位素
Cl2氧化能力相近,二者互为同位素
B.![]() Se与
Se与 ![]() Se所含质子数相同,中子数不同
Se所含质子数相同,中子数不同
C.同主族元素形成的含氧酸的酸性随核电荷数的增加而减弱
D.同周期主族元素形成的简单离子半径随核电荷数的增大而减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图所示的转化关系中,甲为生活中常见的金属单质,乙、丙、丁为气体单质,D为家庭中常用物质(部分反应物和生成物及溶剂水已略去).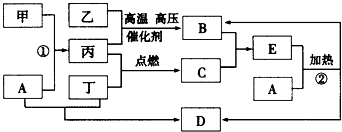
请回答:
(1)E的化学式为;甲的原子结构示意图为;
(2)反应①的离子方程式为;反应②的化学方程式为;
(3)实验室制取并收集B的操作中,用法收集B,验证B已收集满的方法是(限答一种).
(4)实验室制备丁的方程式为 , 工业上输送丁的管道出现气体泄漏,如何查漏(用方程式表示) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com