
| A. | 10 (b-2a) mol•L-1 | B. | 10(2a-b) mol•L-1 | C. | 20(a-2b) mol•L-1 | D. | 20(b-2a) mol•L-1 |
分析 a mol NaOH刚好把NH3全部赶出,根据NH4++OH-═NH3+H2O可知每份中含有amolNH4+,与氯化钡溶液完全反应消耗bmolBaCl2,根据Ba2++SO42-═BaSO4↓可知每份含有SO42-bmol;根据溶液不显电性,计算出每份中Cl-的物质的量,再根据c=$\frac{n}{V}$计算该混合溶液中Cl-物质的量浓度.
解答 解:a mol NaOH刚好把NH3全部赶出,根据NH4++OH-═NH3+H2O可知每份中含有amolNH4+,与氯化钡溶液完全反应消耗bmolBaCl2,根据Ba2++SO42-═BaSO4↓可知每份含有SO42-bmol,
设每份中Cl-的物质的量为x,根据溶液不显电性,则:amol×1=bmol×2+x×1,
解得:x=(a-2b)mol
每份溶液的体积为0.05L,所以每份溶液氯离子的浓度为:c(Cl-)=$\frac{(a-2b)mol}{0.05L}$=20(a-2b)mol•L-1,
故选C.
点评 本题考查物质的量浓度的计算,题目难度中等,明确每份溶液中离子的物质的量浓度与原溶液的关系及溶液中的电荷守恒为解答关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
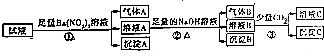
| A. | 试液中一定有Fe2+、SO42-、H+、NH4+、Al3+ | |
| B. | 试液中一定没有Ba2+、CO32-、NO3- | |
| C. | 步骤③中反应的离子方程式为:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- | |
| D. | 气体A、B之间肯定不能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
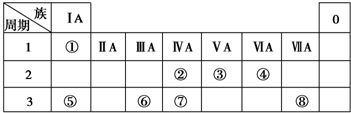
 →
→
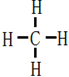 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,说明二氧化硫具有还原性 | |
| B. | 二氧化硫的水溶液中滴加氯化钡无现象,再加入0.5 mL 3%的过氧化氢后产生沉淀 | |
| C. | 二氧化硫能漂白某些物质,说明它具有氧化性 | |
| D. | 二氧化硫漂白过的草帽过一段时间后变黄 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学能转化成光能 | B. | 化学能转化成电能 | ||
| C. | 光能转化成化学能 | D. | 电能转化成光能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有8个中子的氧原子:18O | B. | Na2O的电子式: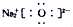 | ||
| C. | HClO 的结构式:H一CI一O | D. | F一的结构示意图: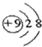 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
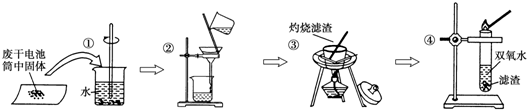
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com